分裂篩選標(biāo)記慢病毒系統(tǒng)
背景介紹
在科研和細(xì)胞工程等領(lǐng)域中構(gòu)建穩(wěn)定表達(dá)細(xì)胞株�����,經(jīng)常需要實(shí)現(xiàn)多個(gè)基因的穩(wěn)定共表達(dá),目前常用的策略是多重感染�����、多重分離篩選等��,然而這種方式存在很多弊端:①真核細(xì)胞中可使用的篩選標(biāo)記數(shù)量有限�����;②實(shí)驗(yàn)周期長(zhǎng)���;③同時(shí)使用多個(gè)不同的篩選基因可能對(duì)細(xì)胞產(chǎn)生不利影響�����;④多基因串聯(lián)��,病毒包裝效率低等;以上問(wèn)題為篩選多基因共表達(dá)的穩(wěn)轉(zhuǎn)株在時(shí)間和成本等方面提出了挑戰(zhàn)���。因此��,有必要開(kāi)發(fā)新的技術(shù)手段解決以上問(wèn)題�����。
維真生物建立了一種可簡(jiǎn)單快速地實(shí)現(xiàn)多基因共表達(dá)的分裂篩選系統(tǒng)�!
分裂篩選標(biāo)記原理
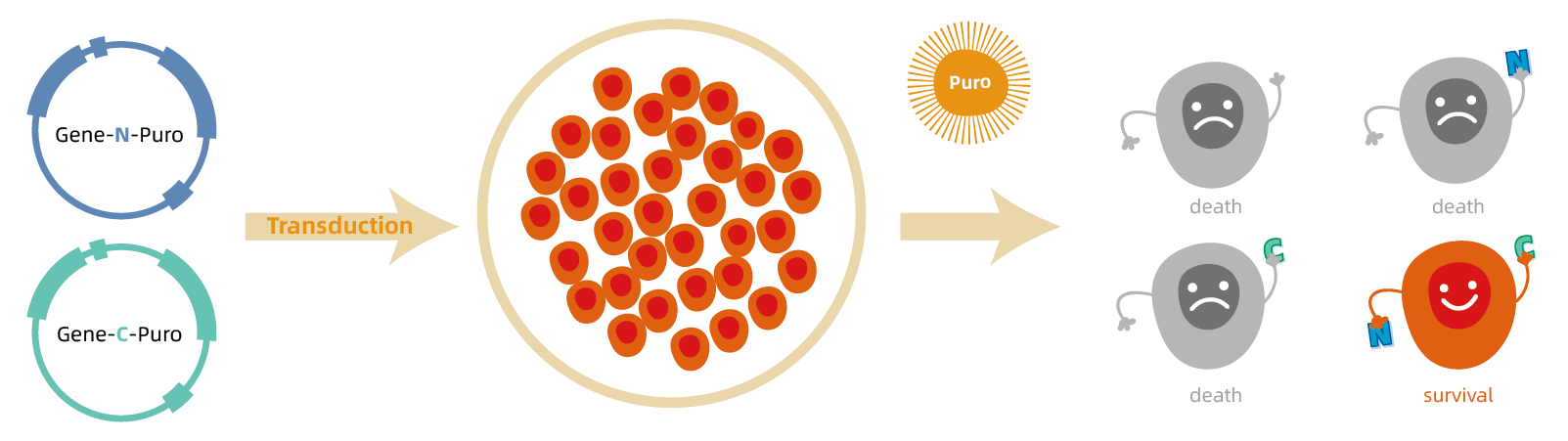
將一種篩選標(biāo)記分成N端和C端兩部分����,分別連接內(nèi)含子剪接接頭TS1和TS2�����,構(gòu)建到兩個(gè)慢病毒載體中��,然后將兩個(gè)載體進(jìn)行細(xì)胞轉(zhuǎn)導(dǎo),部分細(xì)胞在此過(guò)程中“一無(wú)所獲”�,部分細(xì)胞會(huì)“攝取”其中一種載體,部分細(xì)胞會(huì)“攝取”兩種載體�。只有當(dāng)含有N端和C端篩選標(biāo)記的兩個(gè)載體同時(shí)被一個(gè)細(xì)胞“攝取”時(shí),在mRNA水平N-篩選標(biāo)記和C-篩選標(biāo)記才會(huì)連接成一個(gè)完整的篩選標(biāo)記,從而表達(dá)完整的篩選標(biāo)記蛋白����。而那些沒(méi)有“攝取”到載體,或者只“攝取”到一種載體的細(xì)胞(即N端和C端篩選標(biāo)記的兩個(gè)載體沒(méi)有進(jìn)入一個(gè)細(xì)胞)�,該細(xì)胞內(nèi)由于無(wú)法表達(dá)一個(gè)完整的篩選標(biāo)記蛋白,從而被淘汰�。
圖1. 分裂篩選標(biāo)記原理示意圖
研發(fā)路線
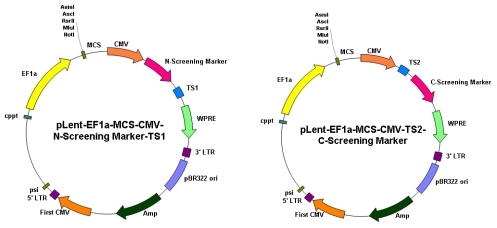
雙載體圖譜
圖2. 慢病毒雙載體圖譜
利用分裂篩選標(biāo)記慢病毒系統(tǒng)快速高效地制備IPS細(xì)胞
誘導(dǎo)性多能干細(xì)胞(IPS cells)是指通過(guò)基因轉(zhuǎn)染技術(shù)(gene transfection)將某些轉(zhuǎn)錄因子導(dǎo)入動(dòng)物或人的體細(xì)胞�����,將終末分化的體細(xì)胞重編程為胚胎干細(xì)胞(ESC)細(xì)胞樣的多潛能細(xì)胞?��,F(xiàn)在大多是通過(guò)病毒攜帶特定的轉(zhuǎn)錄因子進(jìn)入體細(xì)胞內(nèi),來(lái)獲得多能性干細(xì)胞�。2006年日本京都大學(xué)Shinya Yamanaka在世界著名學(xué)術(shù)雜志《細(xì)胞》上率先報(bào)道了誘導(dǎo)多能干細(xì)胞的研究�����,他們把Oct3/4�、Sox2、c-Myc和Klf4這四種轉(zhuǎn)錄因子基因克隆入病毒載體�����,然后引入小鼠成纖維細(xì)胞,發(fā)現(xiàn)可誘導(dǎo)其發(fā)生轉(zhuǎn)化��,產(chǎn)生的iPS細(xì)胞在形態(tài)�、基因和蛋白表達(dá)���、表觀遺傳修飾狀態(tài)、細(xì)胞倍增能力����、類胚體和畸形瘤生成能力���、分化能力等方面都與胚胎干細(xì)胞相似����。
然而���,目前研究人員用來(lái)產(chǎn)生誘導(dǎo)性多能干細(xì)胞的方法耗時(shí)長(zhǎng)且效率低,當(dāng)把四種轉(zhuǎn)錄因子導(dǎo)入成體細(xì)胞如皮膚細(xì)胞中時(shí)���,利用上千個(gè)皮膚細(xì)胞最終只能獲得幾個(gè)iPSCs����。因此�����,我們嘗試?yán)眯陆⒌姆至押Y選標(biāo)記的慢病毒穩(wěn)轉(zhuǎn)系統(tǒng)同時(shí)表達(dá)以上四種轉(zhuǎn)錄因子�����,在短時(shí)間內(nèi)獲得穩(wěn)轉(zhuǎn)細(xì)胞系�。
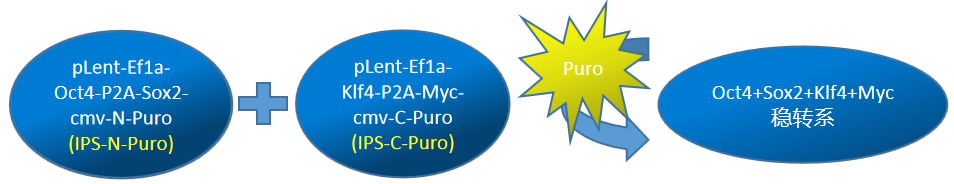
圖3. 利用分裂篩選標(biāo)記慢病毒穩(wěn)轉(zhuǎn)系統(tǒng)篩選IPS穩(wěn)轉(zhuǎn)細(xì)胞系
實(shí)驗(yàn)方案與結(jié)果
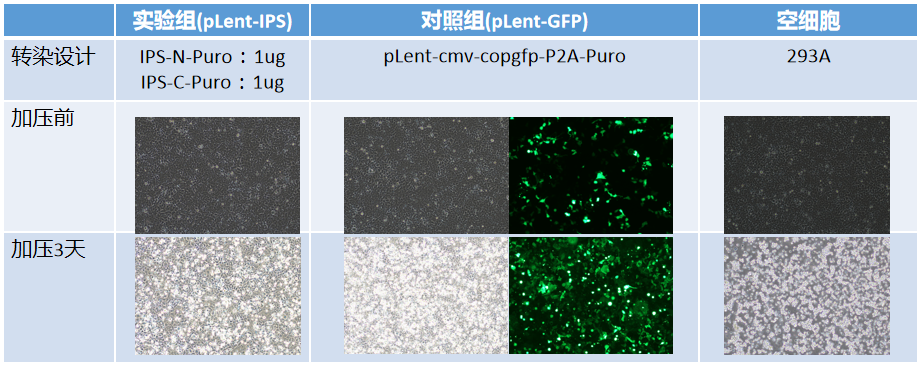
首先,我們將四種轉(zhuǎn)錄因子分成兩組分別構(gòu)建到前面所述的雙慢病毒載體中�,得到pLent-Ef1a-Oct4-P2A-Sox2-cmv-N-Puro(簡(jiǎn)稱IPS-N-Puro)和pLent-Ef1a-Klf4-P2A-Myc-cmv-C-Puro(簡(jiǎn)稱IPS-C-Puro)的慢病毒質(zhì)粒。隨后將這兩個(gè)慢病毒質(zhì)粒共轉(zhuǎn)到293A細(xì)胞中��,通過(guò)Puro篩選����,觀察細(xì)胞生長(zhǎng)情況��。如下圖所示設(shè)置實(shí)驗(yàn)組與對(duì)照組��,我們發(fā)現(xiàn)在Puro加壓后空細(xì)胞組細(xì)胞大量死亡��,而實(shí)驗(yàn)組與對(duì)照組中細(xì)胞存活率較高�。這一結(jié)果說(shuō)明,有大量的雙慢病毒載體進(jìn)入了同一細(xì)胞中����,抗生素基因得到了正常表達(dá)����,大量細(xì)胞得以存活下來(lái)����。
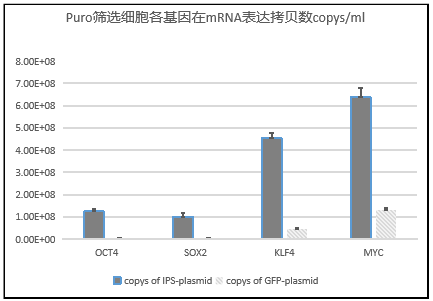
隨后,我們對(duì)實(shí)驗(yàn)組與對(duì)照組細(xì)胞中四種轉(zhuǎn)錄因子mRNA水平的表達(dá)情況進(jìn)行了定量檢測(cè)�,如下圖所示�,我們發(fā)現(xiàn)實(shí)驗(yàn)組細(xì)胞中四種轉(zhuǎn)錄因子的mRNA表達(dá)量都要明顯高于GFP對(duì)照組�����,這一結(jié)果同樣佐證了上述結(jié)論����,有大量的雙慢病毒載體進(jìn)入了同一細(xì)胞中,四種轉(zhuǎn)錄因子實(shí)現(xiàn)了高表達(dá)����。
接著�,我們將上述兩個(gè)慢病毒載體分別包裝成慢病毒����,進(jìn)行293A細(xì)胞的共感染,如下圖所示設(shè)置實(shí)驗(yàn)組和對(duì)照組���,感染72小時(shí)后,加Puro進(jìn)行篩選�����,我們發(fā)現(xiàn)���,空白組細(xì)胞(5)和單一慢病毒感染組(2����、3)的細(xì)胞�����,出現(xiàn)大量死亡,而“攝取”到雙病毒的實(shí)驗(yàn)組(1)和GFP組(4)����,細(xì)胞存活率明顯高于兩病毒單獨(dú)感染組����,在篩選一周后我們成功獲得了大量穩(wěn)轉(zhuǎn)株細(xì)胞�����。
|
慢病毒
|
載體
|
滴度
|
|
IPS-N-Puro
|
pLent-Ef1a-Oct4-P2A-Sox2-cmv-N-Puro
|
7.19E+08 IU/ml
|
|
IPS-C-Puro
|
pLent-Ef1a-Klf4-P2A-Myc-cmv-C-Puro
|
1.87E+09 IU/ml
|
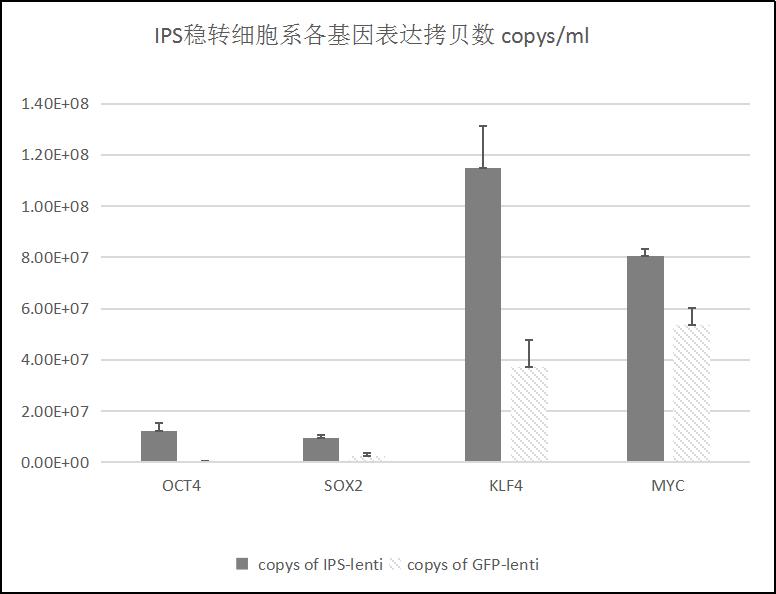
同樣地,我們對(duì)兩病毒共感染組與GFP慢病毒對(duì)照組中細(xì)胞中的四種轉(zhuǎn)錄因子mRNA水平的表達(dá)情況進(jìn)行了定量檢測(cè)�����,結(jié)果與質(zhì)粒轉(zhuǎn)染所得結(jié)果基本一致����,兩病毒共感染組細(xì)胞中四種轉(zhuǎn)錄因子的mRNA表達(dá)量都要明顯高于GFP對(duì)照組,結(jié)果同樣驗(yàn)證了上述結(jié)論���,四基因共表達(dá)的穩(wěn)轉(zhuǎn)株細(xì)胞構(gòu)建成功���。
小結(jié)
維真生物成功建立了一種可實(shí)現(xiàn)分裂篩選標(biāo)記的慢病毒穩(wěn)轉(zhuǎn)系統(tǒng)��,能夠利用一個(gè)篩選標(biāo)記選擇多個(gè)轉(zhuǎn)基因�,使多基因的共同表達(dá)更加簡(jiǎn)單方便,并且能在短時(shí)間內(nèi)進(jìn)行多基因的穩(wěn)轉(zhuǎn)細(xì)胞系構(gòu)建����。目前����,我們已經(jīng)利用該系統(tǒng)成功獲得了四種轉(zhuǎn)錄因子穩(wěn)定表達(dá)的誘導(dǎo)性多能干細(xì)胞的穩(wěn)轉(zhuǎn)細(xì)胞株。此外����,該系統(tǒng)還可以在CRISPR/Cas9基因組編輯中����,用于雙轉(zhuǎn)基因或雙等位基因敲除的陽(yáng)性細(xì)胞選擇。
歡迎各位老師垂詢訂購(gòu)��!