拒絕“肝”擾 ‖ EPHB2有望成為肝細(xì)胞癌治療新靶點(diǎn)
拒絕“肝”擾|EPHB2有望成為肝細(xì)胞癌治療新靶點(diǎn)
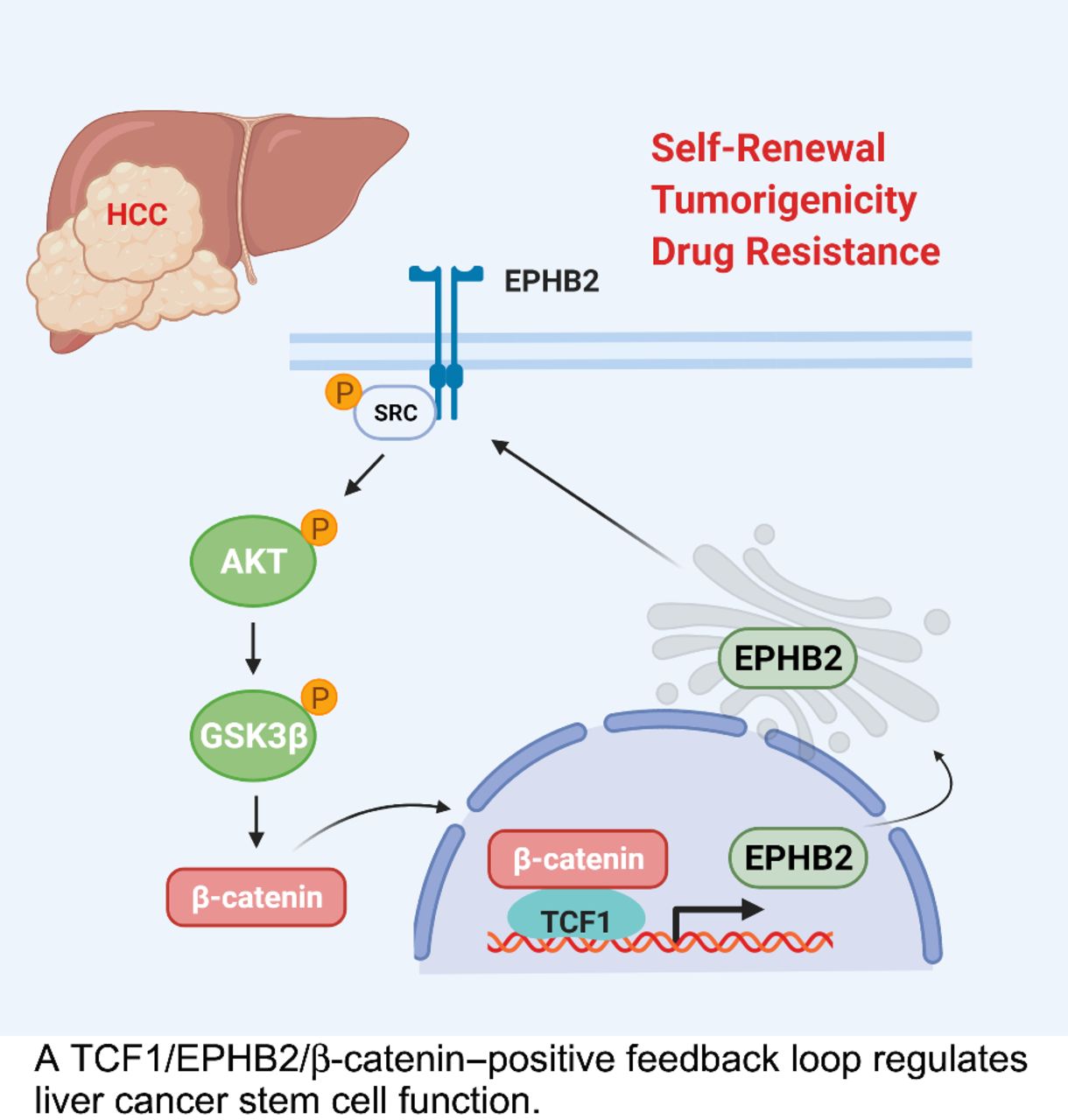
近日��,香港理工大學(xué)李建華教授團(tuán)隊(duì)通過(guò)建立索拉非尼耐藥的HCC(肝細(xì)胞癌)患者源性的腫瘤異種移植模型(PDTXs)����,探究HCC對(duì)索拉非尼的獲得性耐藥機(jī)制,發(fā)現(xiàn)EPHB2激酶在其中起到極其關(guān)鍵的作用��,該研究確定了一個(gè)EPHB2/β-catenin/TCF1的正反饋環(huán)���,可調(diào)節(jié)肝癌的腫瘤干性和對(duì)索拉非尼的耐藥性��,提示靶向該反饋環(huán)可能是對(duì)抗HCC獲得性耐藥的一種可行的治療策略�。
研究背景
肝細(xì)胞癌(Hepatocellular carcinoma, HCC)是全球常見(jiàn)的惡性腫瘤之一����,晚期患者居多且治療效果差、復(fù)發(fā)率高����。2007年索拉非尼獲得FDA批準(zhǔn),成為HCC第一種全身性治療藥物�����,改善了HCC晚期患者的生存率�。然而,由于HCC對(duì)索拉非尼的耐藥性�,生存率并不是十分樂(lè)觀。因此�,深入了解HCC對(duì)索拉非尼的耐藥機(jī)制尤為重要。先前的研究證明�����,對(duì)索拉非尼耐藥的HCC中腫瘤干細(xì)胞(CSC)的干細(xì)胞特性會(huì)增強(qiáng)�,靶向介導(dǎo)肝CSCs特性的信號(hào)通路可能是逆轉(zhuǎn)HCC耐藥的一種策略���。
研究思路
首先���,研究者通過(guò)建立對(duì)索拉非尼耐藥的HCC患者源性的腫瘤異種移植模型(PDTXs),確定了研究靶點(diǎn)——耐藥肝癌細(xì)胞系中上調(diào)最顯著的激酶EPHB2�。經(jīng)測(cè)序及定量分析發(fā)現(xiàn),肝臟CSCs標(biāo)志物在PDTXs中顯著上調(diào)�����,且肝癌組織中EPHB2的表達(dá)明顯高于正常及肝纖維化組織�,提示EPHB2的致癌性。為研究EPHB2在肝癌中的促腫瘤作用�,研究者在免疫活性小鼠中進(jìn)行內(nèi)源EPHB2的敲除,發(fā)現(xiàn)內(nèi)源性EPHB2敲除后腫瘤結(jié)節(jié)的大小和數(shù)量顯著減少���,且小鼠的存活時(shí)間更長(zhǎng)�����。然后研究者進(jìn)行了EPHB2過(guò)表達(dá)和敲除�����,證實(shí)EPHB2表達(dá)升高促進(jìn)了成瘤�����,肝臟CSCs的標(biāo)志物表達(dá)增加����,藥物處理效果較差,而敲除EPHB2后得到與上述相反的結(jié)果���。接著���,研究者探尋上下游效應(yīng)因子,通過(guò)一系列體內(nèi)外實(shí)驗(yàn)�����,最終確定了一個(gè)可以調(diào)節(jié)腫瘤干性與耐藥性的EPHB2/β-catenin/TCF1正反饋環(huán)����。
病毒產(chǎn)品及使用方法
部分研究結(jié)果
該篇研究之初,研究者證實(shí)了EPHB2在索拉非尼耐藥的HCC細(xì)胞中表達(dá)升高�����,并有促腫瘤的作用,能促進(jìn)HCC腫瘤生長(zhǎng)���,參與調(diào)節(jié)肝細(xì)胞癌的CSC特性和耐藥性�����。那么,EPHB2的下游效應(yīng)因子是什么�,其發(fā)揮作用的機(jī)制又是如何���?研究者馬上又進(jìn)行了下一步的探討�����。
RNA測(cè)序分析顯示HCC腫瘤細(xì)胞(PLC/PRF/5)中EPHB2表達(dá)降低后��,Wnt/β-catenin信號(hào)通路中60%以上的相關(guān)基因發(fā)生了顯著改變��。為證實(shí)這一點(diǎn)��,研究者探究了EPHB2突變對(duì)β-catenin反式激活活性的影響����,發(fā)現(xiàn)當(dāng)EPHB2被抑制時(shí)���,β-catenin的反式激活活性被抑制且蛋白表達(dá)量降低�����,EPHB2過(guò)表達(dá)的細(xì)胞則相反���。此外�,免疫沉淀發(fā)現(xiàn)����,EPHB2能磷酸化SRC激酶�,當(dāng)EPHB2被過(guò)表達(dá)或抑制時(shí),SRC的磷酸化會(huì)發(fā)生改變���,進(jìn)而導(dǎo)致AKT/GSK3β/β-catenin信號(hào)通路的變化�。此外��,TCGA分析結(jié)果也顯示W(wǎng)nt/β-catenin信號(hào)通路是EPHB2高表達(dá)的HCC患者中唯一顯著富集的通路���。以上結(jié)果共同證實(shí)��,Wnt/β-catenin是EPHB2的主要信號(hào)因子��。
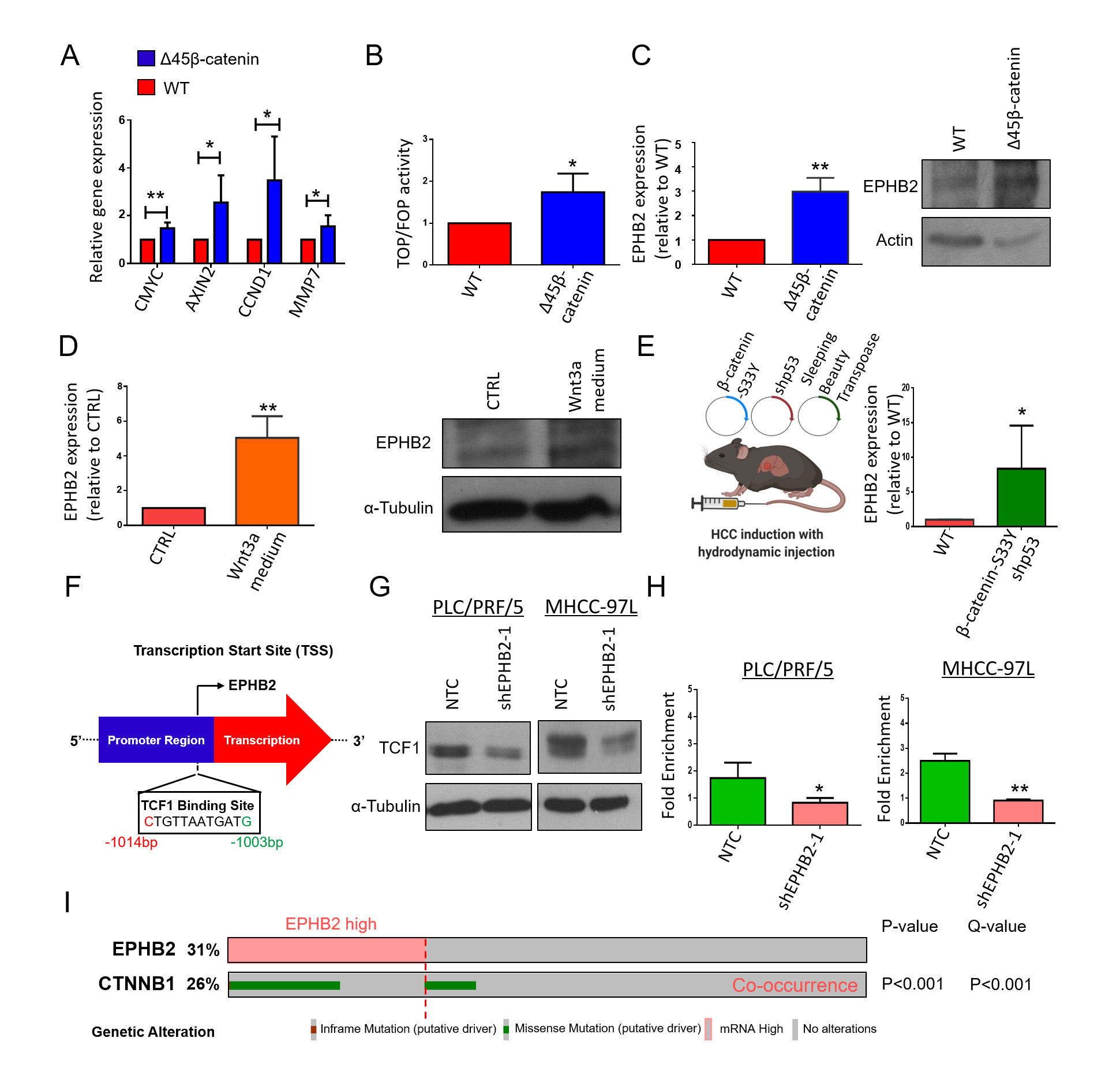
圖1. Wnt/β-catenin是HCC肝癌中EPHB2信號(hào)的下游效應(yīng)因子
已知在結(jié)直腸癌中EPHB2是Wnt的靶基因�,但具體調(diào)節(jié)機(jī)制尚不清楚。研究者通過(guò)體內(nèi)外實(shí)驗(yàn)激活Wnt/β-catenin通路���,發(fā)現(xiàn)EPHB2的表達(dá)水平均呈現(xiàn)持續(xù)上調(diào)����,推測(cè)Wnt/β-catenin在轉(zhuǎn)錄水平激活了EPHB2的表達(dá)����,后通過(guò)生物信息學(xué)的方法預(yù)測(cè)到EPHB2上游存在一個(gè)可能的TCF1(T細(xì)胞因子)結(jié)合位點(diǎn)��,β-catenin可入核與TCF1結(jié)合促進(jìn)EPHB2的轉(zhuǎn)錄表達(dá)�����,形成一個(gè)正反饋回路��。
圖2.EPHB2/β-catenin/TCF1正反饋通路調(diào)節(jié)肝細(xì)胞癌的CSC和耐藥性
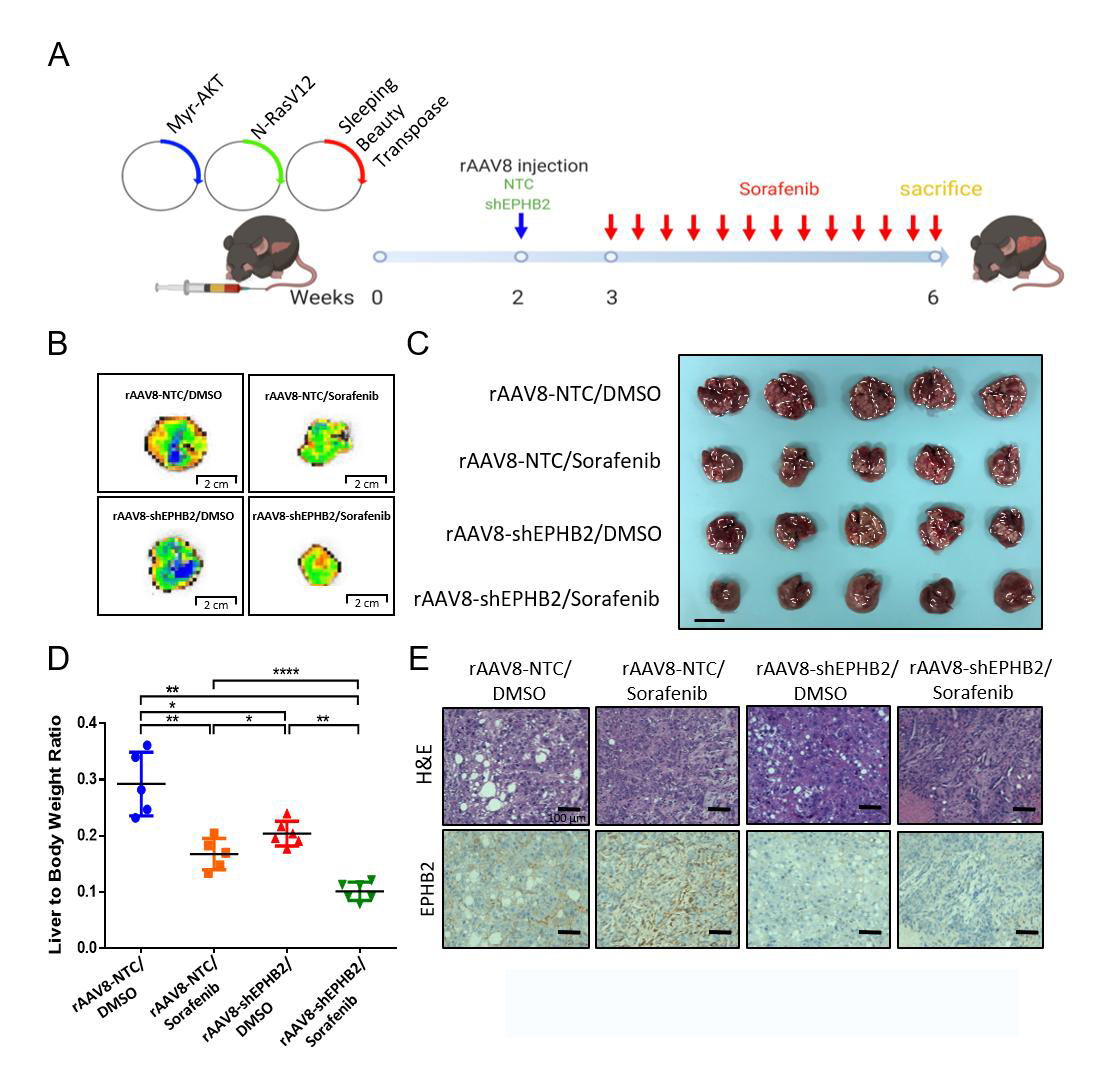
最后��,研究者通過(guò)敲低EPHB2表達(dá)并聯(lián)合索拉非尼探究EPHB2體內(nèi)治療的靶向性��。在NRAS/ akt誘導(dǎo)肝癌小鼠模型兩周后�,通過(guò)靜脈注射rAAV8-shEPHB2(維真生物榮幸提供)抑制EPHB2的表達(dá),并在一周后給予小鼠30mg /kg的索拉非尼治療21天(DMSO作為對(duì)照藥物)���。通過(guò)計(jì)算實(shí)驗(yàn)組與對(duì)照組小鼠的肝重/體重比�,研究者發(fā)現(xiàn)rAAV8- shEPHB2聯(lián)合索拉非尼對(duì)腫瘤生長(zhǎng)有明顯的抑制作用����,說(shuō)明降低EPHB2表達(dá)并聯(lián)合索拉非尼協(xié)同治療能有效抑制體內(nèi)HCC的發(fā)生。
圖3.敲低EPHB2可增強(qiáng)HCC細(xì)胞對(duì)索拉非尼的敏感性
小結(jié)
綜上所述�����,該研究證明EPHB2通過(guò)TCF1/EPHB2/β-catenin正反饋環(huán)來(lái)調(diào)節(jié)腫瘤的干性和耐藥性���。靶向EPHB2或與其他靶點(diǎn)聯(lián)合治療肝癌可能是一種新的治療策略。