AAV在腦組織中的靶向策略(干貨篇)
神經(jīng)系統(tǒng)分為中樞神經(jīng)系統(tǒng)(Central nervous system, CNS)和外周神經(jīng)系統(tǒng)(Peripheral nervous system,PNS)��。中樞神經(jīng)系統(tǒng)包括腦和脊髓����,分別位于顱腔和椎管內(nèi),是神經(jīng)系統(tǒng)的主要部分���,外周神經(jīng)系統(tǒng)包括與腦相連的腦神經(jīng)(cranial?nerves)和與脊髓相連的脊神經(jīng)(spinal?nerves)���。隨著研究的深入����,人們對神經(jīng)系統(tǒng)功能已經(jīng)有了更近一步的認識�,但由于神經(jīng)系統(tǒng)的復雜性��、組織再生能力的有限性以及血腦屏障對藥物傳送的阻隔,使用傳統(tǒng)藥物和外科手術(shù)方法治療神經(jīng)系統(tǒng)類疾病仍困難重重。
人腦解剖圖
目前�����,基因療法已被應用于多種疾病的治療���,利用病毒載體將遺傳物質(zhì)傳遞到器官周圍�����,并在靶細胞中實現(xiàn)特異表達�,進而實現(xiàn)基因治療���。在神經(jīng)科學研究中��,尤其是在體實驗����,通常利用腺相關(guān)病毒工具載體研究基因的功能作用�����,那么如何才能更高效地利用AAV在神經(jīng)系統(tǒng)進行基因轉(zhuǎn)導呢�?今天我們就一起學習AAV在神經(jīng)研究中的選擇策略����。
一�、AAV血清型的選擇
據(jù)報道�,目前適用于神經(jīng)系統(tǒng)的AAV血清型有:1�、2�����、5、6、8���、9、PHP.B���、PHP.eB��、PHP.S、DJ����、Retro����、rh10等十幾種,不同的血清型在神經(jīng)系統(tǒng)不同部位的感染效率及擴散能力不同����,合適的血清型關(guān)乎基因是否能夠?qū)崿F(xiàn)高效穩(wěn)定表達�����,甚至關(guān)乎最終的研究結(jié)果���,因此綜合標記的細胞和每種AAV血清型的特性等因素來選擇合適的AAV血清型至關(guān)重要����。根據(jù)文獻報道,AAV1,2和5在CNS轉(zhuǎn)導水平有限����,且表現(xiàn)出不同的細胞特異性��,如AAV1和5能轉(zhuǎn)導神經(jīng)元和膠質(zhì)細胞�,而AAV2只能轉(zhuǎn)導神經(jīng)元���。AAV9在CNS中的應用則較為廣泛���,具有強的擴散性�,且能穿過血腦屏障(BBB)實現(xiàn)基因高表達���。而在外周神經(jīng)系統(tǒng)中�����,AAV9��、rh10��、PHP.S的感染效果較好�。
接下來���,就來詳細介紹一下在神經(jīng)環(huán)路示蹤中幾種常用的AAV血清型:
1���、可逆向示蹤的血清型— AAV2-retro
常見的AAV病毒載體都是順向標記�,極少能進行逆行傳遞,這大大限制了AAV載體在神經(jīng)環(huán)路示蹤中的應用�����。直到2016年���,研究人員在AAV2的基礎(chǔ)上�����,通過定向進化的方式改造出一種具有逆向示蹤功能的AAV2突變體——AAV2-retro,該載體能夠在小鼠大腦中進行有效的神經(jīng)環(huán)路逆向標記,且其逆行示蹤能力和效率與傳統(tǒng)的逆行示蹤劑相當���。圖2所示為rAAV2-retro的開發(fā)過程及應用實例:
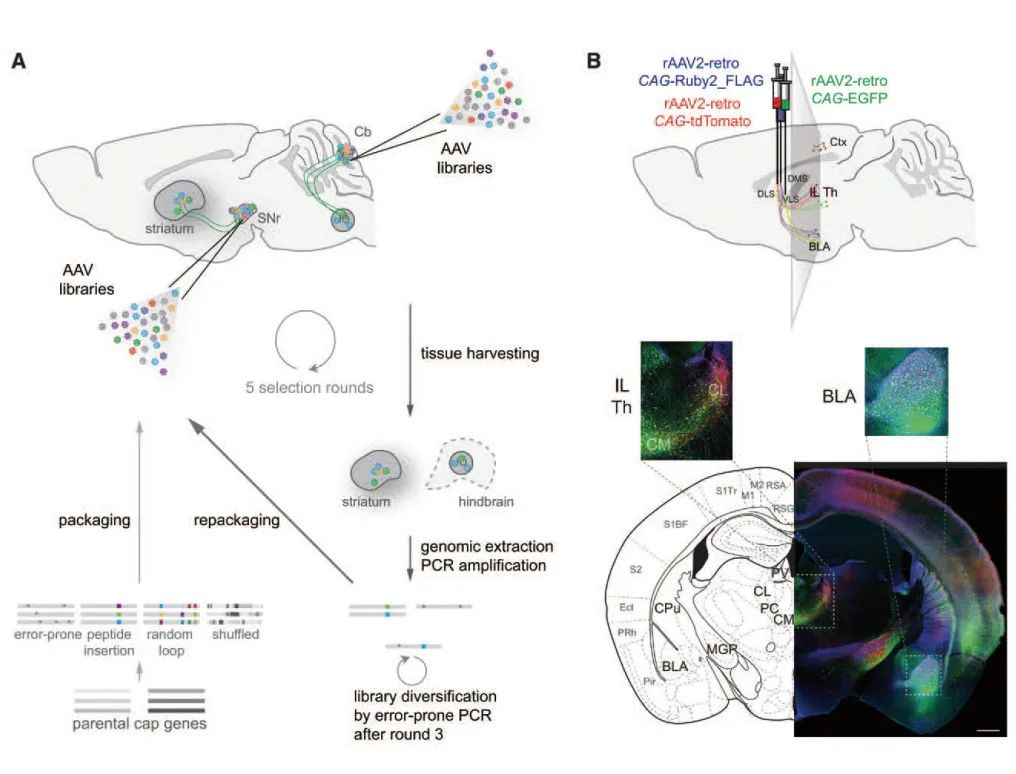
rAAV2-retro(逆向非跨突觸標記)
(Tervo et al., Neuron, 2016)
2�、可順向跨單級突觸的血清型 — AAV1
2017年張礪教授團隊研究報道AAV1能在高滴度條件下呈順向跨突觸傳播���,與Cre依賴的報告系統(tǒng)相結(jié)合����,可高效和特異性地驅(qū)動Cre依賴的外源基因在突觸后神經(jīng)元中的表達����,以標記突觸后神經(jīng)元����。2020年該研究團隊再次深入研究了AAV1順向跨突觸標記的作用機制——依賴于突觸囊泡的釋放���,同時揭示了其在多種神經(jīng)環(huán)路中的廣泛應用,為AAV1作為順向跨突觸示蹤病毒工具對神經(jīng)元及其投射腦區(qū)進行標記提供了諸多證據(jù),如圖3所示����。
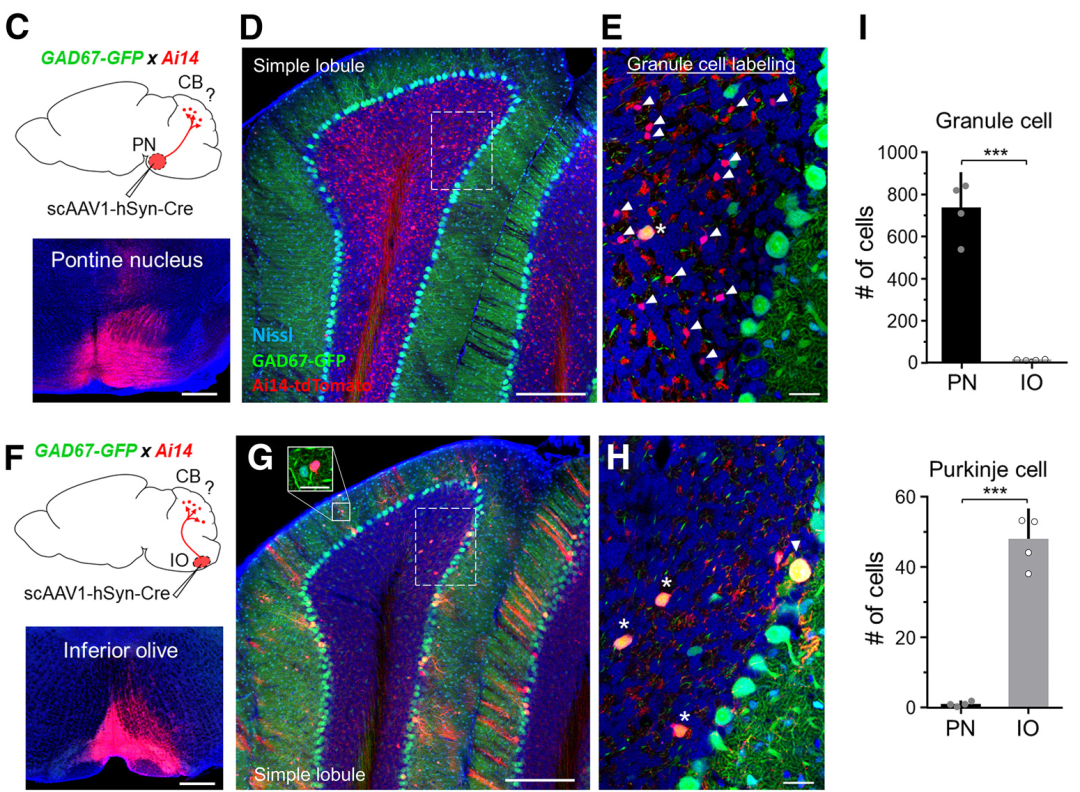
AAV1順向跨突觸標記
(Zingg B et al., J Neurosci, 2020)
此外,張礪教授團隊還證實scAAV1-hSyn-Cre相比AAV1載體具有更優(yōu)越的順向跨突觸標記能力�����,可在興奮性、抑制性、神經(jīng)調(diào)質(zhì)和腦-脊髓等多種神經(jīng)環(huán)路中有效�����、特異地標記單突觸靶神經(jīng)元及其輸出���,從而解析不同的功能/行為。
3���、可跨血腦屏障的血清型 — AAV9�����、AAVPHP.B����、AAVPHP.eB���、AAVPHP.S��、AAV.CPP.16
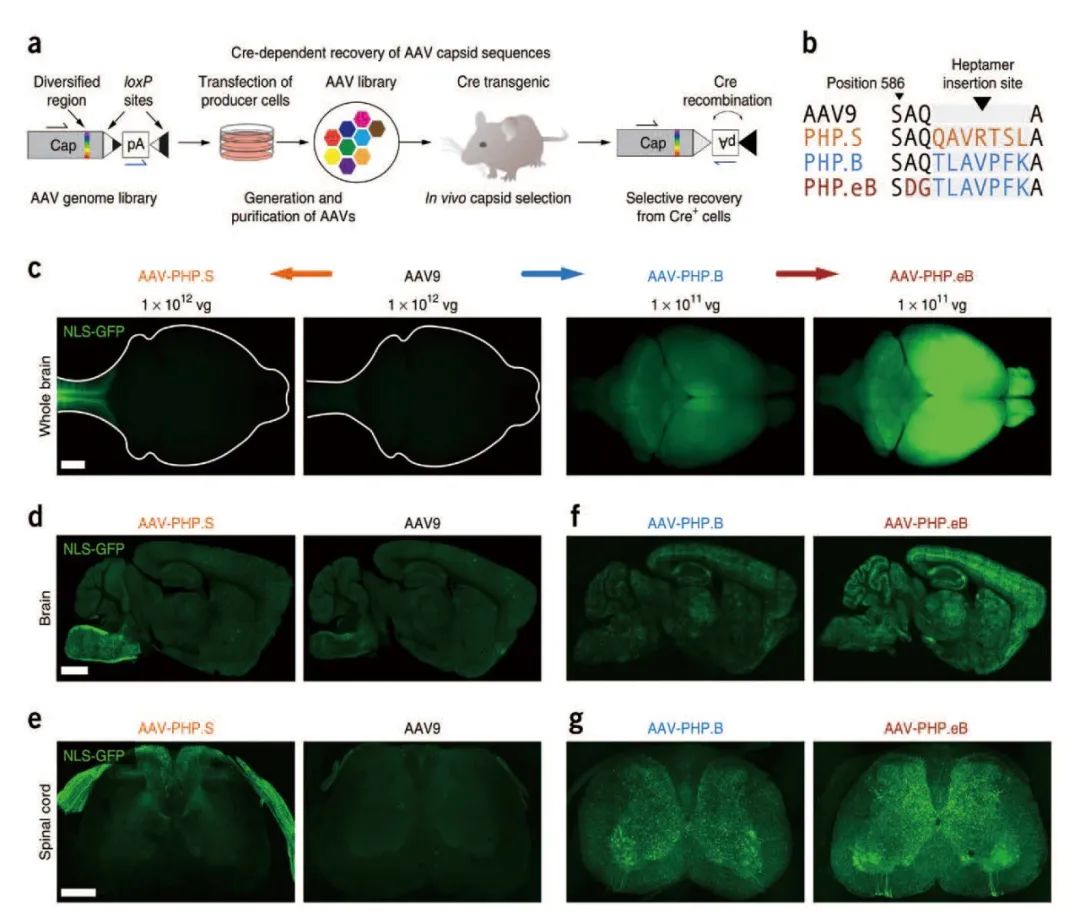
血腦屏障的存在對中樞神經(jīng)系統(tǒng)有很強的保護作用,但同時它也能阻隔藥物的傳遞和吸收,使神經(jīng)系統(tǒng)疾病的治療變得異常困難�,研究人員通過進一步改造AAV衣殼,發(fā)現(xiàn)AAV9& AAVPHP.B&AAVPHP.eB&AAVPHP.S可以有效介導基因由外周向中樞神經(jīng)系統(tǒng)的跨越���,繼而將遺傳物質(zhì)遞送至大腦或脊髓中。研究結(jié)果顯示�,AAV-PHP.B可以有效地轉(zhuǎn)導成年小鼠大腦和脊髓的神經(jīng)元���,AAV-PHP.eB降低了誘導大多數(shù)中樞神經(jīng)系統(tǒng)神經(jīng)元所需的病毒載量�����,而AAV-PHP.S顯示出對周圍神經(jīng)元的更好趨向性�����??傊@些AAV變體可以有效介導基因由外周向中樞神經(jīng)系統(tǒng)的跨越���,更好地應用于神經(jīng)環(huán)路研究。
AAV9& AAVPHP.B& AAVPHP.eB& AAVPHP.S有效介導基因由外周至中樞神經(jīng)系統(tǒng)的跨越
(Ken Y Chanet al., Nat Neurosci, 2017)
美國哈佛大學聯(lián)合武漢大學人民醫(yī)院研究團隊利用合理性設(shè)計的方法,將選定的細胞穿透肽 CPP(一 組可以穿過細胞膜或組織屏障的短肽)分別插入 AAV9 衣殼(Q588 和 A589 之間)生成突變體庫��, 將包裝好的 AAV 突變體通過靜脈注射至小鼠體內(nèi),經(jīng)過序列優(yōu)化和篩選測試��,得到血腦屏障穿透性顯著優(yōu)于 AAV9 的 AAV.CPP.16��。通過在不同品系小鼠和食蟹猴動物模型中進行驗證,發(fā)現(xiàn)靜脈注射AAV.CPP.16 可以高效跨越血腦屏障����,感染 CNS 神經(jīng)元細胞��、星形膠質(zhì)細胞以及脊髓運動神經(jīng)元��。基于小鼠與食蟹猴研究結(jié)果發(fā)現(xiàn)����,系統(tǒng)給藥 AAV.CPP.16 仍可感染肝臟�����、肌肉����、心臟等外周臟器����,但在檢查的組織中均未觀察到明顯的病理反應���,也未引起背根神經(jīng)節(jié)退化變性。重要的是����,研究人員發(fā)現(xiàn)AAV.CPP.16 可用于 GBM 小鼠模型的基因治療�,并具有持久高效的抗腫瘤作用。
AAV.CPP.16 對食蟹猴的腦部轉(zhuǎn)導效率顯著優(yōu)于AAV9
啟動子:CAG 實驗動物:新生食蟹猴(3 月齡)/ 成年食蟹猴(3-4 歲)
注射方式:靜脈注射 病毒用量:新生食蟹猴 2×10E13vg/kg�,成年食蟹猴 5×10E13vg/kg
(Yao et al., Nat Biomed Eng, 2022)
4���、可高效靶向神經(jīng)元細胞的血清型—AAV.CAP-B10
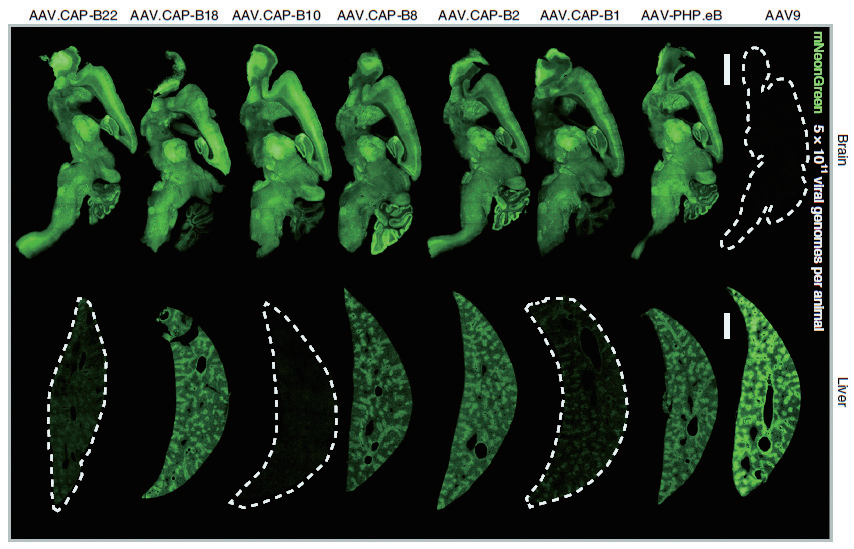
加州理工學院的 Viviana Gradinaru 團隊通過對 AAV9 進行衣殼改造,開發(fā)了一系列 AAV 變體,其中AAV.CAP-B10�����,靜脈注射后�,不僅能夠突破血腦屏障�����,高效靶向神經(jīng)元細胞�����,同時不會在肝臟富集���。
該研究團隊對比了不同 AAV 血清型通過靜脈注射在各組織器官中的遞送效率�����,結(jié)果發(fā)現(xiàn),AAV. CAP-B10 表現(xiàn)出對中樞神經(jīng)系統(tǒng)的特異性,高度靶向神經(jīng)元細胞�����,對肝臟具有低靶向性,這一結(jié)果不僅在小鼠上得到了證實��,在非人靈長類動物狨猴上也得到了證實。這為腦研究工作者提供了新的工具策略,同時這也為腦部疾病提供了一種更安全����、有效的治療選擇�。
AAV.CAP-B10 高效靶向小鼠腦組織而非肝臟
啟動子:CAG 實驗動物:雄性 C57BL/6J 小鼠
注射方式:靜脈注射 病毒用量:5×1011VG/mice
(David Goertsen et al., Nature Neuroscience, 2022)
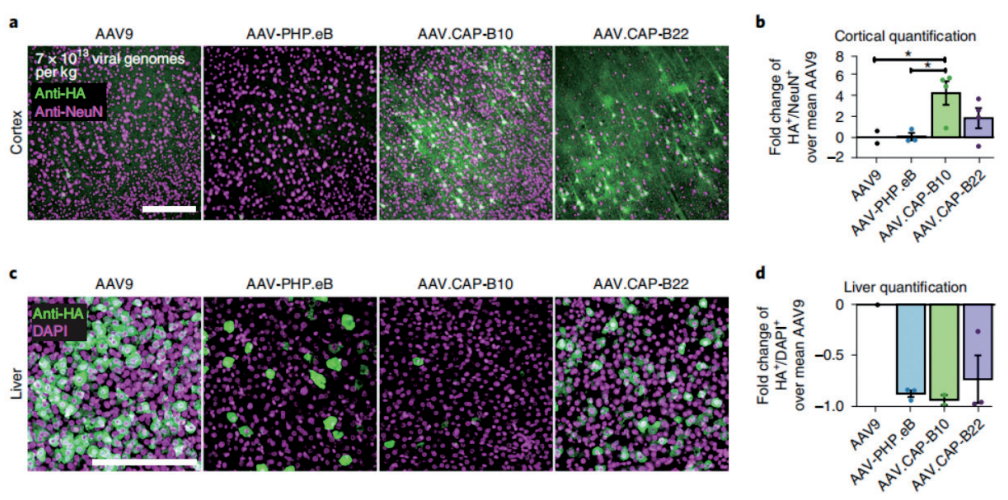
在狨猴中��,AAV.CAP-B10 特異性靶向神經(jīng)元
啟動子:CAG���;實驗動物:成年狨猴;
注射方式:靜脈注射����;病毒用量:7×1013VG/KG
(David Goertsen et al., Nature Neuroscience, 2022)
5、可高效靶向星形膠質(zhì)細胞的血清型—rAAV11
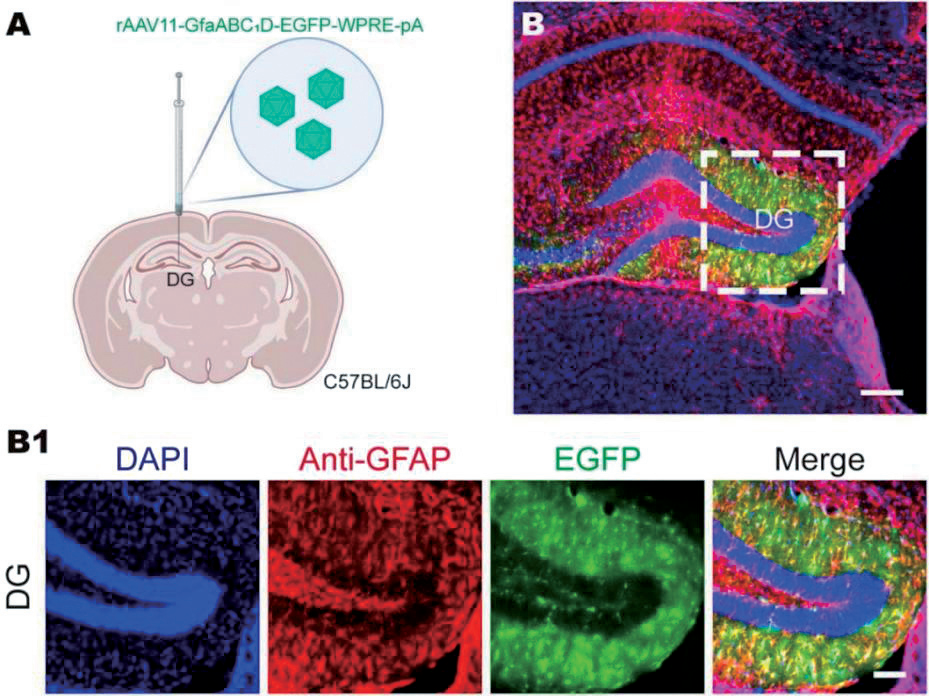
星形膠質(zhì)細胞是中樞神經(jīng)系統(tǒng)損傷的關(guān)鍵反應細胞���,在脊髓損傷的發(fā)病機制中發(fā)揮著重要作用�����。星形膠質(zhì)細胞功能障礙已被證實是腦卒中���、阿爾茨海默病�����、帕金森病和亨廷頓病等神經(jīng)退行性疾病的核心特征��。中科院徐富強團隊對一系列工具病毒進行改造和篩選�����,開發(fā)了一種新的高效逆行靶向投射神經(jīng)元的重組腺相關(guān)病毒 rAAV11���。研究發(fā)現(xiàn)�����,rAAV11 可以高效逆行靶向投射神經(jīng)元���,且不表現(xiàn)出順行跨突觸特征;rAAV11 還具備優(yōu)秀的逆行標記效率��,能示蹤 rAAV2 難以轉(zhuǎn)導的投射神經(jīng)元�。值得注意的是�,rAAV11 可以高效且特異性靶向星形膠質(zhì)細胞��,為星形膠質(zhì)細胞的研究提供了更加有力的病毒工具。
rAAV11 靶向星形膠質(zhì)細胞
啟動子:GfaABC1D;實驗動物:C57BL/6J 小鼠����;
注射部位:齒狀回(DG)區(qū)�����;病毒用量:2×109 VG/mice
(Han et al., bioRxiv preprint, 2022)
6���、可高效靶向小膠質(zhì)細胞的血清型—AAV-cMG & AAV-MG
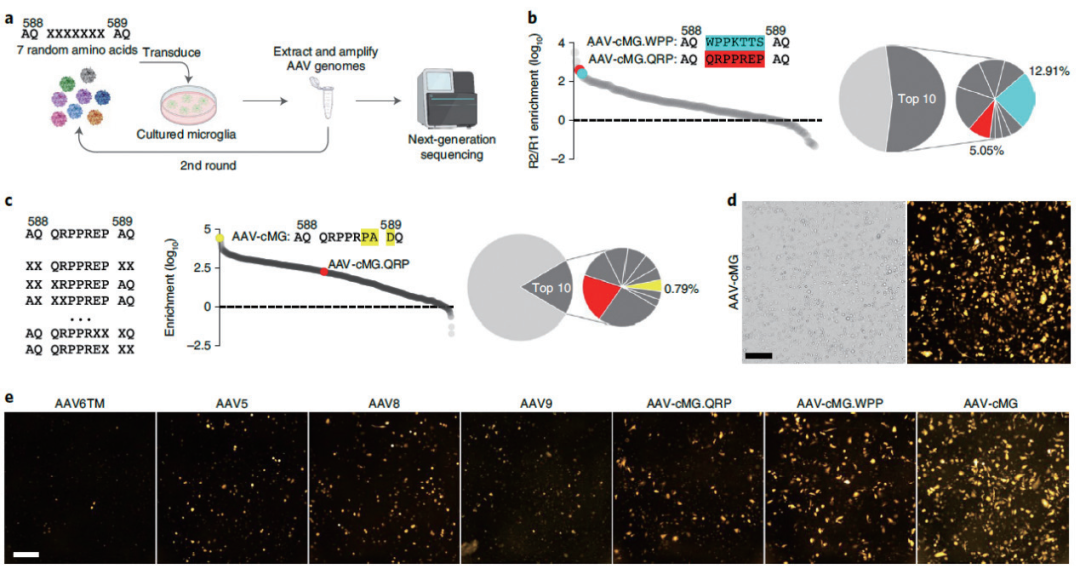
北京生命科學研究所羅敏敏實驗室通過定向進化策略,開發(fā)了一系列能夠在體內(nèi)和體外高效侵染小膠質(zhì)細胞的新型 rAAV 載體�����。該研究針對 AAV9 的衣殼蛋白進行改造,鑒定篩選出兩個衣殼蛋白(AAV-cMG. WPP 和 AAV-cMG.QRP)能夠在一定程度上提高 rAAV 病毒對體外培養(yǎng)的小鼠小膠質(zhì)細胞的侵染效率�����。以此為基礎(chǔ)�����,研究團隊針對 AAV-cMG.QRP 的插入肽段及其在衣殼蛋白插入位點的相鄰氨基酸進行突變篩選���,成功得到了高效侵染體外培養(yǎng)小膠質(zhì)細胞的 AAV-cMG 衣殼蛋白�����,同時并不導致小膠質(zhì)細胞的激活。
體外篩選得到 AAV-cMG
啟動子:CMV�;轉(zhuǎn)染細胞:小膠質(zhì)細胞�����;MOI:104
(Lin et al., Nature Neuroscience, 2022)
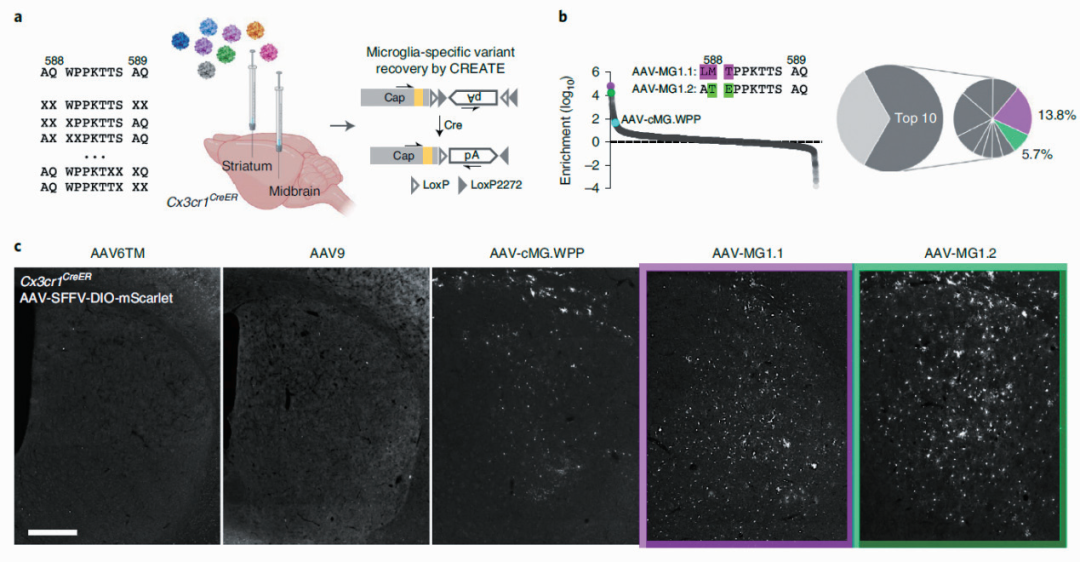
研究人員進一步在 AAV-cMG.WPP 基礎(chǔ)之上構(gòu)建新的 AAV 突變文庫����,并在小膠質(zhì)細胞特異的 Cx3cr1-CreER 轉(zhuǎn)基因小鼠腦內(nèi)進行針對性體內(nèi)篩選��,成功鑒定得到 AAV-MG1.1 和 AAV-MG1.2�����,能夠在體內(nèi)高效侵染小膠質(zhì)細胞�,且不誘導小膠質(zhì)細胞免疫激活��。
體內(nèi)篩選得到 AAV-MG1.1/1.2 高效轉(zhuǎn)導小膠質(zhì)細胞
啟動子:CMV��;實驗動物:Cx3cr1-CreER 轉(zhuǎn)基因小鼠�;
注射部位:紋狀體(800nl)和中腦(500nl)����;
病毒滴度:5×107 vg.μl-1
(Lin et al., Nature Neuroscience, 2022)
這兩類分別適用于體外侵染培養(yǎng)小膠質(zhì)細胞(AAV-cMG)和體內(nèi)侵染內(nèi)源性小膠質(zhì)細胞(AAV-MG)的新型 rAAV 載體�����,將有助于小膠質(zhì)細胞生物學及相關(guān)疾病機制的研究。
7�����、可高效靶向中樞血管內(nèi)皮細胞的血清型—AAV-BI30
腦血管內(nèi)皮細胞是表達在血管腔隙的一類中樞非神經(jīng)元細胞群體��,作為血腦屏障的重要組成部分����,參與許多關(guān)鍵的生理過程�。美國麻省理工學院-哈佛大學布羅德研究所的 Benjamin E. Deverman 組和哈佛醫(yī)學院的 ChenghuaGu組開發(fā)了一種新的血清型 AAV-BI30�,可在多個鼠系體內(nèi)以及體外高效轉(zhuǎn)導內(nèi)皮細胞�����。在相對較低的全身劑量下�����,該載體可轉(zhuǎn)導成年 C57BL/6 小鼠大腦���、視網(wǎng)膜和脊髓血管系統(tǒng)中的大多數(shù)動脈���、毛細血管和靜脈內(nèi)皮細胞����。
AAV-BI30 能有效地通過動靜脈軸轉(zhuǎn)導大腦內(nèi)皮細胞
啟動子:CAG����; 實驗動物:成年 C57BL/6J 小鼠�;
注射方式:靜脈注射�����; 病毒用量:1×1011 vg/mice
(Krolak et al., NATuRE CARDIoVASCuLAR RESEARCH,2022)
AAV-BI30 靶向視網(wǎng)膜和脊髓血管系統(tǒng)的內(nèi)皮細胞
啟動子:CAG�����;實驗動物:成年 C57BL/6J 小鼠����;
注射方式:靜脈注射;病毒用量:1×1011 vg/mice
(Krolak et al., NATuRE CARDIoVASCuLAR RESEARCH, 2022)
此外�,AAV-BI30 在 CNS 中能實現(xiàn)高效的 Cre 介導的基因操縱�����。AAV-BI30 能高效的在中樞不同類型血管內(nèi)皮細胞中特異性表達�����,適用于神經(jīng)血管生物學相關(guān)研究�����,并有助于開發(fā)內(nèi)皮功能障礙類疾病的治療方法。
二、AAV載體的優(yōu)化選擇(ssAAV or scAAV)
根據(jù)細胞類型與實驗目的選擇好合適的血清型后���,還可以進行實驗需要進行AAV載體的優(yōu)化選擇����。腺相關(guān)病毒為單鏈DNA病毒(ssAAV), 在入核���、脫衣殼后�����,需要借助宿主DNA聚合酶或者分子間退火完成雙鏈轉(zhuǎn)化�,才能啟動基因轉(zhuǎn)錄過程,這一過程限制了AAV載體介導的基因轉(zhuǎn)導��,并直接影響病毒的感染效率。自身互補雙鏈DNA的腺相關(guān)病毒(scAAV)能夠克服這一限制�,不需要經(jīng)歷一個由單鏈變?yōu)殡p鏈的過程,也就是說�����,雙鏈AAV病毒進入細胞后,可以直接表達���,并且表達時間更快�����,表達水平更高。因此���,在神經(jīng)研究中��,也可以根據(jù)需要選擇scAAV載體�,完成目的基因更快表達,或者基因更強表達的研究����。
三、啟動子的選擇
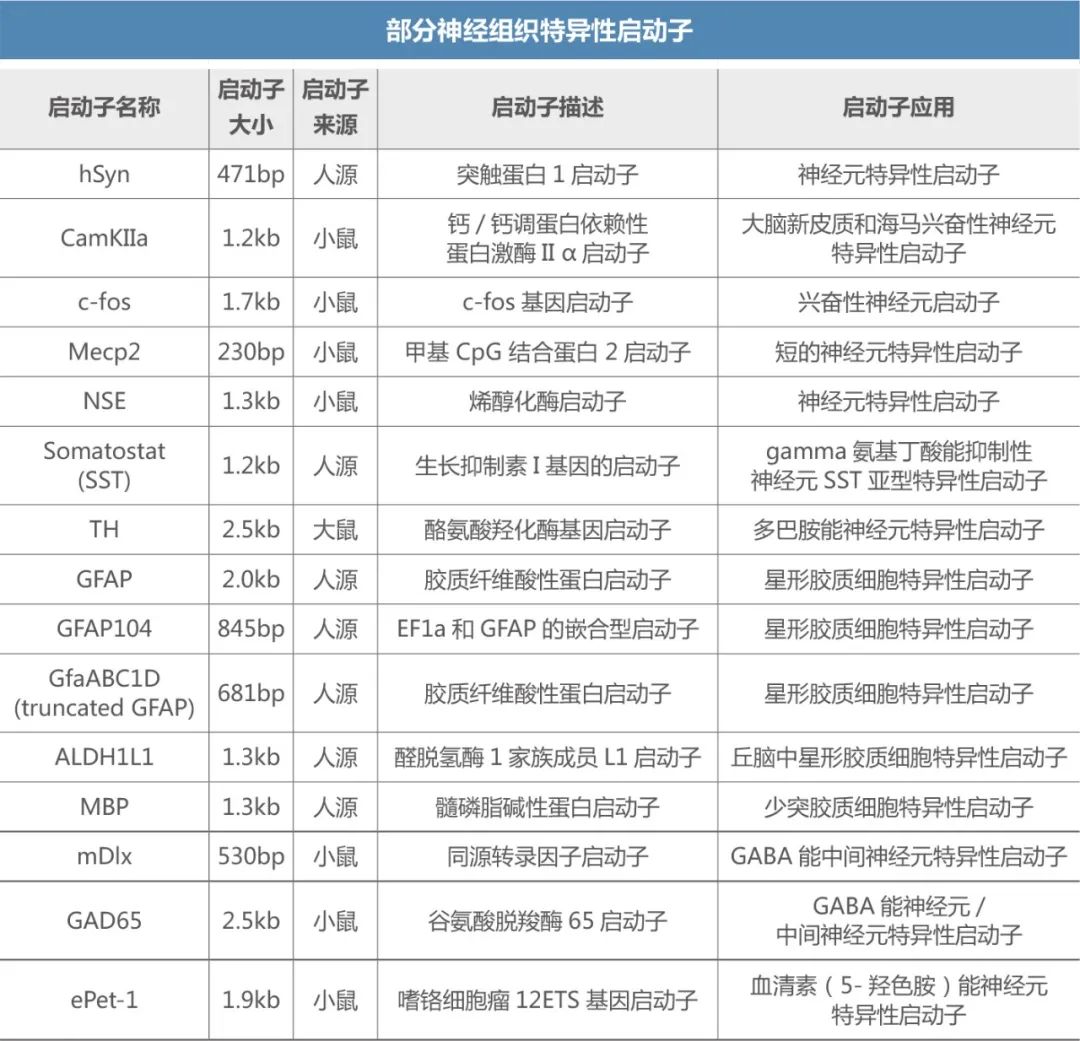
除了AAV載體與血清型����,啟動子和調(diào)控元件的優(yōu)化也十分必要����。目前,研究中使用的廣譜型啟動子����,如巨細胞病毒啟動子CMV��、CMV增強子融合的雞?-肌動蛋白啟動子CAG等,可實現(xiàn)目的基因的高表達。四環(huán)素啟動子TRE作為誘導型啟動子����,則可以在特定條件下啟動基因的表達。然而�,神經(jīng)系統(tǒng)的組成極其復雜�,腦部的精密研究非常關(guān)鍵�����,要想實現(xiàn)某個腦區(qū)甚至是某一類細胞的特異性感染,選擇一種特異性相對更強的啟動子尤為重要�。
常見的神經(jīng)組織特異性啟動子
四�、轉(zhuǎn)錄后調(diào)控元件的添加
AAV載體上轉(zhuǎn)錄后調(diào)控元件的添加��,對于mRNA的剪接及核輸出、mRNA的穩(wěn)定性及翻譯等具有重要意義���,下面列舉兩個對于提高外源基因表達非常重要的轉(zhuǎn)錄后調(diào)控元件�。
1��、內(nèi)含子
真核mRNA內(nèi)含子在真核生物基因表達調(diào)控中起著重要的作用����,是轉(zhuǎn)基因研究中提高外源基因表達的重要元件之一��。在多數(shù)情況下,真核mRNA內(nèi)含子的存在可以提高基因的表達水平�,因為其剪接過程會影響mRNA新陳代謝的多個階段���,包括轉(zhuǎn)錄、RNA編輯����、pre-mRNA的加工、mRNA的出核運輸�、翻譯等。所以說�����,在載體容量允許的情況下可添加一個內(nèi)含子,有助于刺激基因的表達��。
2����、WPRE元件
土撥鼠肝炎病毒轉(zhuǎn)錄后調(diào)節(jié)序列WPRE是一段順式作用的RNA元件�����,放在多聚腺苷酸化信號之前可顯著增加mRNA的表達水平和翻譯效率,進而增強基因的表達�����,并且WPRE插入病毒載體中還可以大大提升病毒包裝的滴度����。然而由于WPRE序列較長(600bp左右)�,所以還需要視具體的載體容量選擇性插入。
五�����、注射方式的選擇
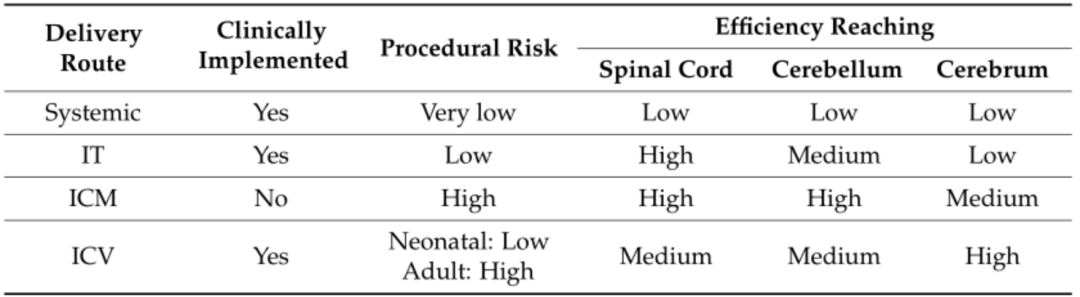
目前AAV在神經(jīng)系統(tǒng)研究中的注射方法主要有以下幾種:腦實質(zhì)內(nèi)注射����、靜脈注射��、腦室注射(ICV)����、枕大池內(nèi)注射(ICM)和鞘內(nèi)注射(IT)����,其中ICV、ICM和IT注射是通過腦脊髓液進行傳遞�����。每種注射方式各有優(yōu)缺點����,研究者可根據(jù)具體的研究對象以及實驗方案,選擇適合的注射方式�,推薦進行預實驗對實驗效果做初步測試��,以得到更優(yōu)的選擇方案��。
四種常用AAV神經(jīng)給藥特點
(Ocana-Santero G et al. ����,International Journal of Molecular Sciences, 2021)
下面介紹幾種常用注射方法及相應的病毒注射劑量:
(1)腦立體定位注射
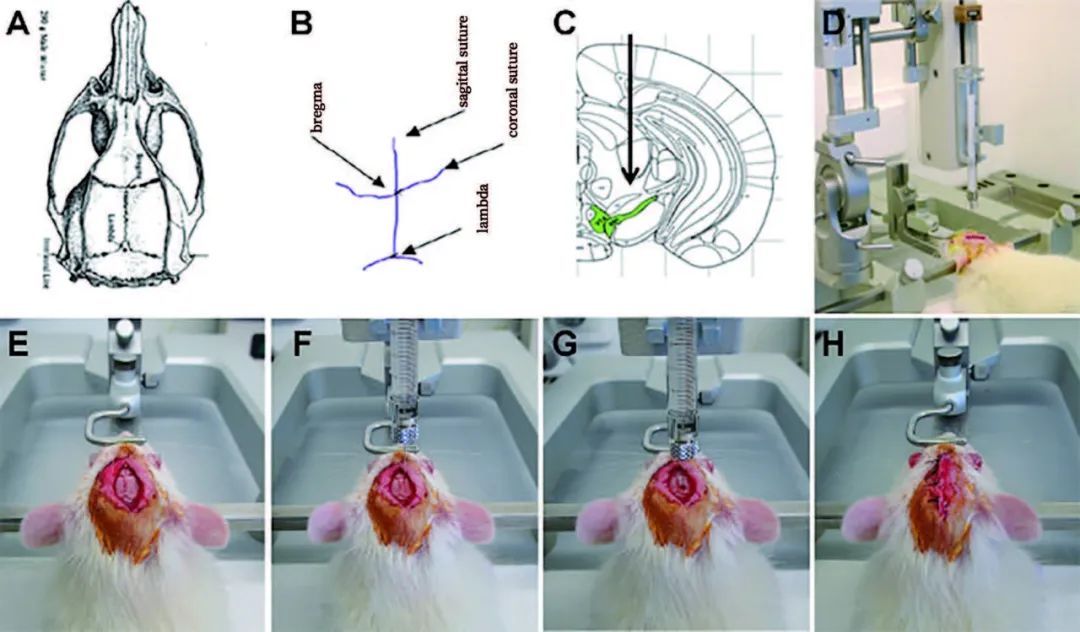
腦立體定位注射,相比其他注射方式靶向性強����,注射病毒體積小�,但是侵入性也強�,且對操作者具有很高的要求。在立體定位手術(shù)時��,顱骨上常用的注射參照點是前囟,也就是中矢狀冠狀縫的交叉點(下圖B中的十字交叉點)。具體操作步驟如下:
1. 實驗動物稱重����,進行麻醉����;
2. 待實驗動物完全麻醉后���,用剃毛器將動物頭頂眼睛至耳朵之間的毛發(fā)剃除干凈;
3. 將麻醉后的實驗動物固定于腦立體定位儀上���;
具體操作為:實驗動物眼部涂抹青霉素眼藥膏以保護其雙眼�����;將門齒掛在門齒掛鉤上��,確保頭部保持固定;檢查左右耳桿是否在同一水平上�,將左右耳桿通過外耳道插入實驗動物耳內(nèi)�。實驗動物固定好的標準為:鼻對正中,頭部不動����,提尾不掉���,目測大腦放置水平;
4. 手術(shù):用碘伏/ 無色葡萄糖氯己定溶液對實驗動物頭皮進行消毒清理,用手術(shù)刀沿中間位置剪開頭皮����,用鑷子對表面的結(jié)締組織進行清理�,暴露實驗動物的顱骨表面��;然后進行調(diào)平��,首先找到前囟這個坐標����,并將其歸零�,然后向左右調(diào)平�����,使左右兩側(cè)處于同一水平����,調(diào)整前后囟�����,使前后囟也在同一水平;
5. 病毒注射:通過查詢實驗動物的腦立體定位圖譜確定待注射腦區(qū)的位置(下方圖片是大鼠和小鼠的腦譜)�,并確定其坐標值,即ML 值(X 軸)��、AP 值(Y 軸)���、DV 值(Z 軸)�����;根據(jù)目標腦區(qū)設(shè)定好坐標��,移開注射針����,用顱骨鉆開窗( 由于顱骨薄, 故務必注意顱骨鉆的力度?��?!), 操作時避免傷及腦組織;微量注射器吸取病毒液���,隨后固定在定位儀上����,根據(jù)設(shè)好的坐標進行病毒注射,注射速度控制在0.1-0.15μL/min�����,注射劑量視具體實驗而定。注射完畢���,留針10min����,以便病毒液充分吸收����,然后慢慢回針;
6. 縫合頭皮并消毒, 完成腦定位注射; 將動物從腦立體定位儀取下, 回籠待蘇醒; 動物蘇醒后,正常喂養(yǎng), 病毒注射后2-4 周可檢測轉(zhuǎn)基因的表達����。
提示:若手術(shù)麻醉時間較長�����,建議不要用酒精消毒,防止酒精揮發(fā)導致動物體溫過低而死亡�。手術(shù)過程和蘇醒過程注意保暖。
腦立體定位注射示意圖
(Van der Perren A et al. JOVE-J VIS EXP. 2016)
(2)鞘內(nèi)注射
與系統(tǒng)注射和實質(zhì)內(nèi)注射相比���,鞘內(nèi)給藥是一種具有較低劑量要求的微創(chuàng)替代方法����。步驟如下:
1�、使用毛巾覆蓋在小鼠頭部和背部,露出髂嵴以下的腰部區(qū)域����;用非慣用手的拇指和食指抓住鼠的髂骨(髖骨)�,手的頂部輕輕放在小鼠身體和頭部上����,使其保持平靜。
注:在髂骨上的握力應該足夠強�����,以固定小鼠的腿部活動����,并使腿部向外和向下伸展�。
2��、使用慣用手食指從腰椎到骶部沿脊柱輕輕按壓����,同時使用非慣用手輕輕上拉小鼠�����,以打開椎節(jié)之間的空間�����,方便進針����。
3���、將1 ?”號針的斜面指向小鼠頭部,然后將針以70°角插入脊柱中線的腰椎處�,當感覺針碰到骨頭時�����,將針的角度調(diào)整到30°夾角�����,并將針插入椎節(jié)之間��。
注:需多次嘗試找到合適的進入點�,針頭進入脊柱后推針沒有阻力��,尾巴或后腿的反射性彈跳出現(xiàn)時�,說明已正確入針。
4�����、輕輕壓下注射器的活塞���,將5-10μL的AAV病毒懸液注射至蛛網(wǎng)膜下腔�。
注:注射時間控制在10-30s較好,速度太快會導致小鼠后腿抽筋�����,該現(xiàn)象會在60s內(nèi)消失����。
5����、注射后��,將針180°旋轉(zhuǎn)1-2次,然后將針從脊柱中取出。
6��、小鼠放回籠子觀察,確認恢復正常運動功能�����。
注:此法適用于成年小鼠或大鼠。
(3)靜脈注射
系統(tǒng)性給藥方式�����,侵入性較小,但是相比其他注射方式特異性也較差�,因此所需病毒體積更大���。步驟如下:
新生小鼠的顳靜脈注射
1����、調(diào)整光源位置以便照亮顯微鏡區(qū)域,中等強度的光照為佳。
2�����、將一個新生幼鼠直接置于冰上1-3min���,進行麻醉�。
3、當動物在冰上麻醉時����,在注射器中注滿AAV病毒�,注射體積不應超過100μL�。
4���、在顯微鏡下觀察幼鼠。用不持注射器的手的食指放在幼鼠口鼻處���,中指放在耳芽處�����,以便拉伸幼鼠的皮膚�����,可見顳淺靜脈���。
5����、確定顳淺靜脈�����。可通過皮膚看到位于耳芽前部��,周圍毛細血管下部,有一條隱約可見的靜脈血管�,從背部到腹部�,匯入頸靜脈,這就是顳淺靜脈���。
6、注射器針尖斜面插入顳靜脈�?���?梢钥吹结樇庑泵嫱ㄟ^皮膚的以后被血填充����。輕壓注射器���,并注意幼鼠臉側(cè)面的靜脈變白��。
成年小鼠眶后靜脈注射
1����、注射異氟醚對小鼠進行麻醉,使用非慣用手手掌握住小鼠背部��,將拇指放在氣管正側(cè)面����,頭部皮毛攏至手掌,使小鼠眼球凸起����。
2、將手腕支撐在穩(wěn)定的表面上,用拇指����、中指和無名指握住注射器����,將食指放在柱塞上方。
3、對小鼠施加輕微壓力使眼睛凸出��,針頭對準內(nèi)眥,斜面朝外�����,將針頭以45°插入眶后竇中心約5mm�����;
4�����、使用0.5ml 28G注射器緩慢注入150-200μL病毒懸液;
5���、緩慢地取出針頭,確保針頭不會劃傷眼角膜�����。使用無菌紗布止血�����,并在眼睛上涂抹藥膏助其恢復。
6��、注射后��,將小鼠放回籠中恢復直至清醒����。
成年小鼠眶后靜脈注射
(Gessler D J et al. Methods Mol Biol. 2019 )
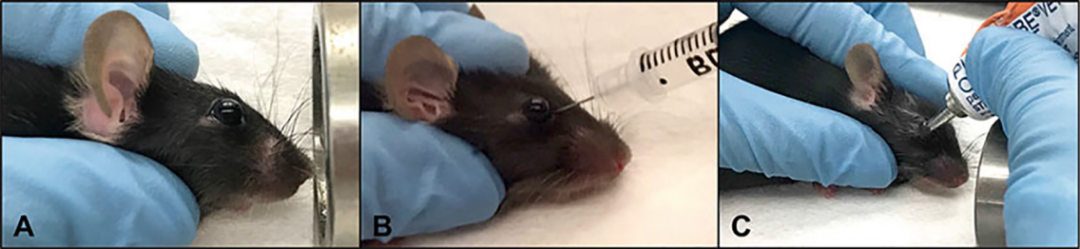
尾靜脈注射
1、將小鼠放入約束器中���,使尾巴從開口處露出�����。避免過度限制小鼠��,以免導致其呼吸受阻。
2�����、在尾部涂抹70%異丙醇�。
3�����、將小鼠尾巴拉直�����,可看到尾巴兩側(cè)各有一條側(cè)脈。
4�、將針尖以30°角插入側(cè)靜脈中���。一旦針尖穿過了靜脈的一半,重新調(diào)整針頭����,使其與靜脈的長度一致(圖3c)��。如果針頭插入正確��,則按壓注射器注射時應無阻力。
5���、使用0.5ml 28G注射器緩慢注射300μLAAV病毒懸液�����,此時靜脈顏色會變白,大約4s后����,顏色恢復正常���。
6��、小心將針頭取出�,用吸水紗布按壓注射部位10秒進行止血�����。
7����、將小鼠放回籠子��。

尾靜脈注射
(Gessler D J et al. Methods Mol Biol. 2019 )
小結(jié)
值得注意的是�����,除了以上所述各項因素外����,AAV病毒本身的滴度和純度��,目的基因本身的自然屬性(如胞內(nèi)蛋白/分泌蛋白/轉(zhuǎn)運蛋白)以及AAV感染后所使用的檢測方法等因素也會影響到基因最終的表達效果。因此,在神經(jīng)系統(tǒng)研究中�,想要驅(qū)動更高效的基因轉(zhuǎn)導���,可以綜合考慮以上各項因素�����,優(yōu)化選擇����。
AAV在腦組織中的靶向策略(應用篇)(可點擊查看)