蛋白磷酸化攻略大全
前幾日�,我們?yōu)榇蠹医榻B了關(guān)于反相蛋白微陣列RPPA的有關(guān)知識(『江湖召集令』癌癥相關(guān)蛋白及磷酸化水平大數(shù)據(jù)等你來分析?。肦PPA技術(shù)可以同時分析成百上千種細(xì)胞或者組織樣本中不同蛋白的表達(dá)情況��,包含修飾后蛋白(如磷酸化�、甲基化�����、乙?���;┑牟町惐磉_(dá)比對分析�����,那么,關(guān)于蛋白質(zhì)翻譯后修飾你了解多少呢�,蛋白質(zhì)磷酸化究竟又是怎么一回事?今天��,小V就和大家一起來探索有關(guān)蛋白質(zhì)磷酸化的那些事兒��!
蛋白質(zhì)翻譯后修飾(PTMs)在生命體中具有十分重要的作用,它使蛋白質(zhì)的結(jié)構(gòu)更復(fù)雜���,功能更完善,調(diào)節(jié)更精細(xì)��,作用更專一���。蛋白翻譯后修飾包括:磷酸化��、糖基化、甲基化����、羥基化����、脂?��;Ⅳ然裙矁r修飾��。其中,蛋白磷酸化是非常常見和非常重要的翻譯后修飾之一��,它在每個生物的各個方面都扮演著重要的角色���,例如基因轉(zhuǎn)錄�����、表達(dá)、細(xì)胞增殖��、分化、凋亡�、信號轉(zhuǎn)導(dǎo)��、免疫調(diào)控、腫瘤發(fā)生等�����。
一.蛋白磷酸化簡介
蛋白磷酸化是在酶的催化作用下����,將ATP γ位的磷酸基團(tuán)���,轉(zhuǎn)移至蛋白質(zhì)氨基酸側(cè)鏈上的過程���。該過程是可逆的�����,催化蛋白質(zhì)發(fā)生磷酸化的酶被稱為蛋白激酶(protein kinase, PK)���,而催化蛋白質(zhì)去磷酸化的酶被稱為蛋白磷酸酶(protein phosphatase, PPase)(圖1)��。蛋白磷酸化是調(diào)節(jié)和控制蛋白質(zhì)活性和功能的重要機(jī)制�����。
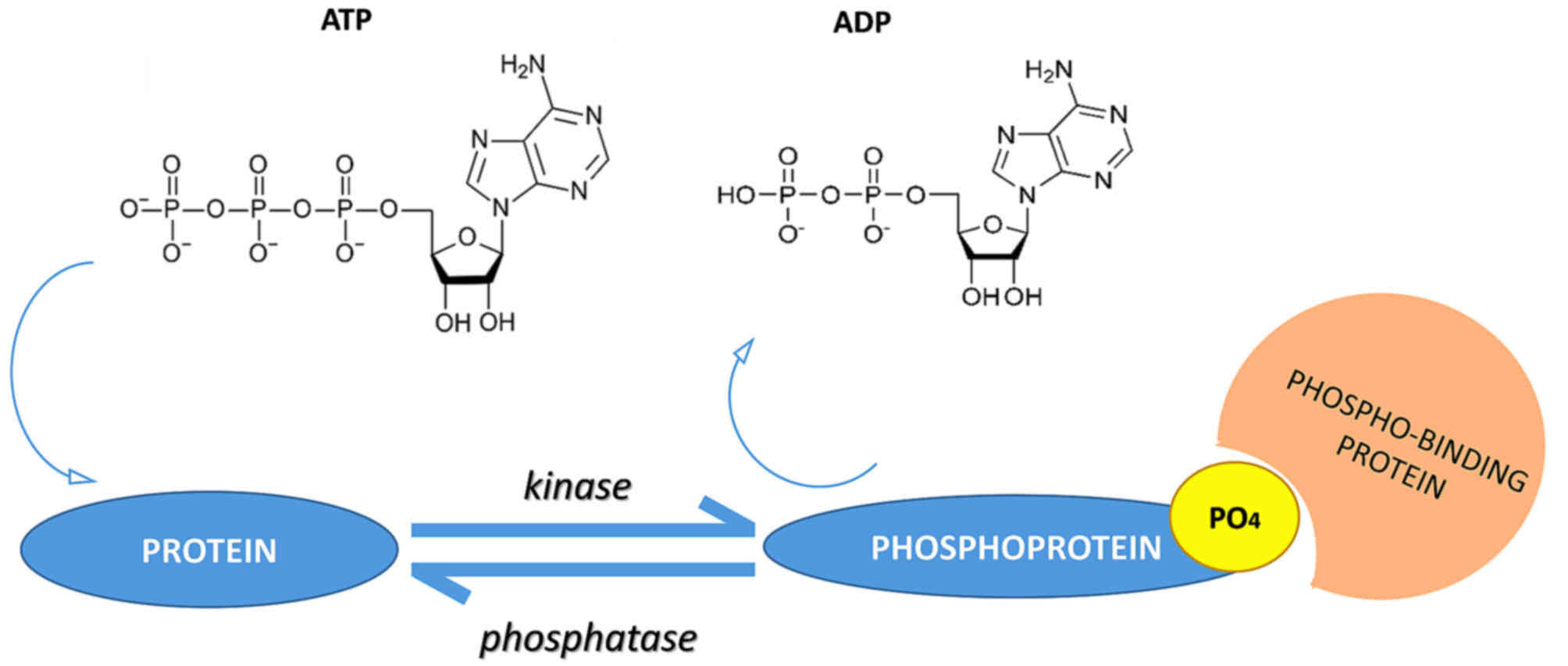
圖1:蛋白質(zhì)磷酸化和去磷酸化的過程(圖片來源于網(wǎng)絡(luò))
二.蛋白磷酸化分類及位點(diǎn)
蛋白磷酸化是生物體內(nèi)普遍存在的一種調(diào)節(jié)方式�����。據(jù)報(bào)道���,人類基因組編碼的21000個蛋白質(zhì)中��,90%以上發(fā)生了磷酸化��。根據(jù)被磷酸化的氨基酸殘基不同,蛋白質(zhì)磷酸化可分為 4 大類���,具體分類和磷酸化位點(diǎn)見表1,磷酸化的9個氨基酸分子式見圖2。超過三分之一的蛋白磷酸化發(fā)生在絲氨酸����、蘇氨酸和酪氨酸殘基上:其中絲氨酸殘基最多(86.4%),其次是蘇氨酸殘基(11.8%)����,酪氨酸殘基最少(1.8%)。絲氨酸����、蘇氨酸和酪氨酸的磷酸化組成了O-磷酸化。O-磷酸化在酸性條件下非常穩(wěn)定���,因此在細(xì)胞生物學(xué)和磷酸化蛋白質(zhì)組學(xué)中研究廣泛�。而N-磷酸化由于不穩(wěn)定導(dǎo)致其檢測極具挑戰(zhàn)性。加之���,催化N-磷酸化的蛋白激酶和蛋白磷酸酶的缺乏進(jìn)一步限制了它的研究���。其他兩類磷酸化(S-磷酸化和酰基磷酸化)的研究報(bào)道卻少之又少�����。
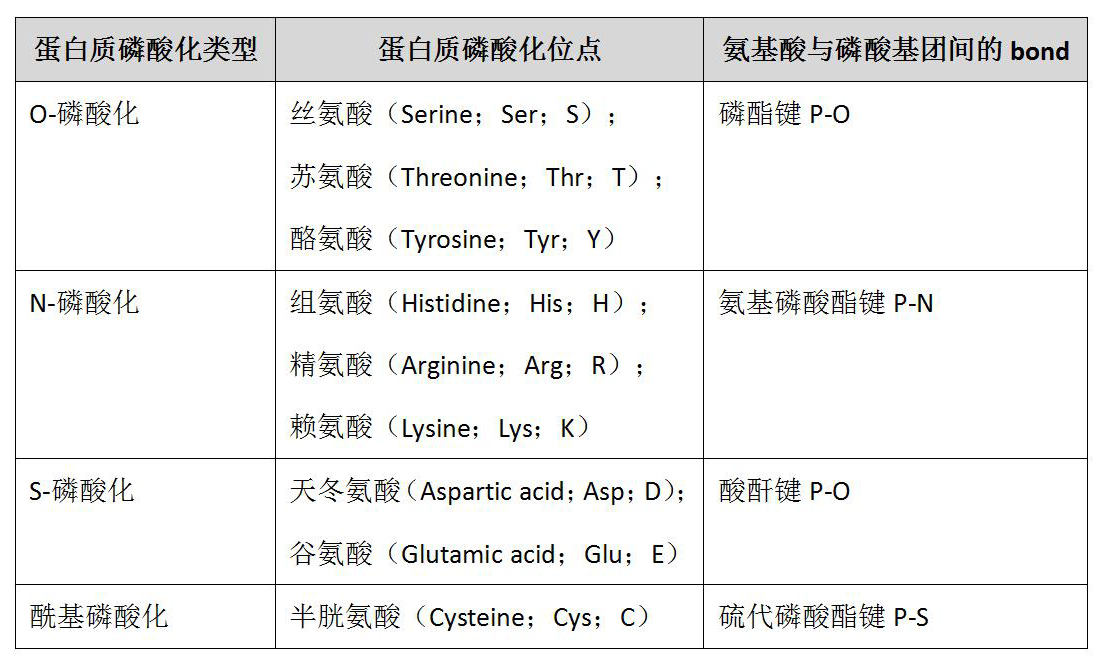
表1:蛋白磷酸化類型及位點(diǎn)
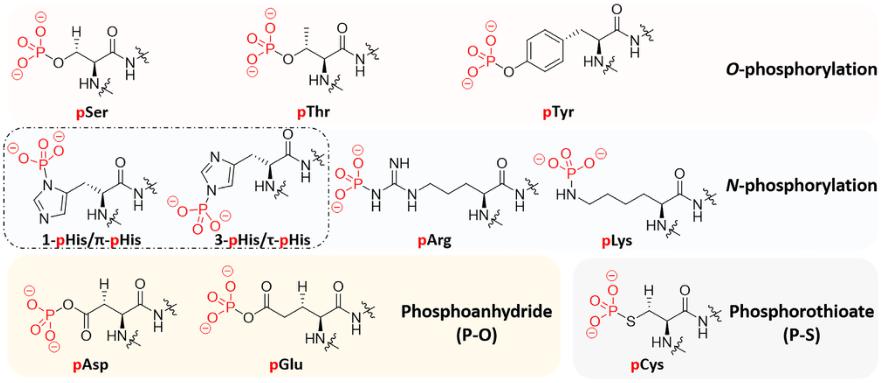
圖2:磷酸化的9個氨基酸分子式
(B. Huang et al. International Journal of Biological Macromolecules 145 .2020)
三.蛋白磷酸化相關(guān)酶
人類基因組中約有500多種激酶和200多種磷酸酶能調(diào)控蛋白的磷酸化過程��,這使得蛋白磷酸化更為復(fù)雜,這些磷酸化相關(guān)酶在精細(xì)調(diào)控生物體的眾多細(xì)胞過程中可發(fā)揮關(guān)鍵作用�。
1�、蛋白激酶
蛋白激酶屬于激酶大家族���,是一類磷酸轉(zhuǎn)移酶����,負(fù)責(zé)將ATP γ位的磷酸基團(tuán)轉(zhuǎn)移至底物蛋白質(zhì)的特定氨基酸�����,從而使蛋白質(zhì)磷酸化�����,進(jìn)而發(fā)揮生理生化功能�����。在人類基因組中,大約2%的人源基因編碼518個蛋白激酶����。根據(jù)其磷酸化的氨基酸殘基不同����,蛋白激酶可以分為五大類:絲氨酸/蘇氨酸蛋白激酶���、酪氨酸蛋白激酶、組氨酸/賴氨酸/精氨酸蛋白激酶�、半胱氨酸蛋白激酶和天冬氨酸/谷氨酸蛋白激酶��。
2��、蛋白磷酸酶
蛋白磷酸酶的功能跟蛋白激酶的功能相反����,負(fù)責(zé)磷酸化蛋白的去磷酸化���。目前����,大約有226種已知的蛋白磷酸酶。蛋白磷酸酶分為3個家族:磷酸蛋白磷酸酶家族���、金屬依賴性蛋白磷酸酶家族和蛋白酪氨酸磷酸酶家族。
四.蛋白磷酸化的檢測方法
蛋白質(zhì)磷酸化的分析和磷酸化位點(diǎn)的鑒定已成為目前蛋白質(zhì)組學(xué)研究的關(guān)注點(diǎn)之一����。目前蛋白質(zhì)磷酸化的檢測方法主要有特異性抗體(如western blot)��、p32放射性標(biāo)記�����、質(zhì)譜��、化學(xué)生物相結(jié)合、核磁共振等��。每種方法有其各自的優(yōu)缺點(diǎn)(表2),研究人員可根據(jù)實(shí)驗(yàn)設(shè)計(jì)挑選合適的檢測方法��。
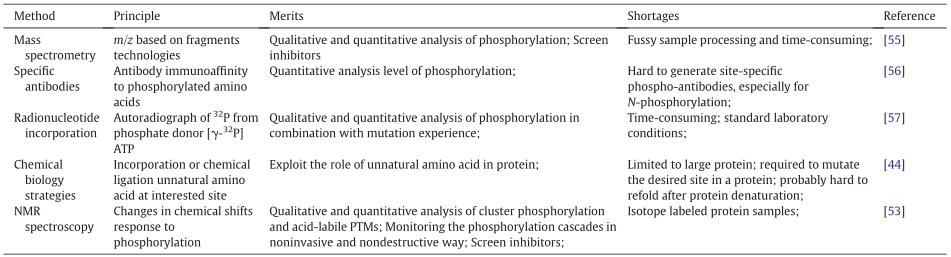
表2:蛋白質(zhì)磷酸化檢測方法的比較
(B. Huang et al. International Journal of Biological Macromolecules 145 .2020)
五.定點(diǎn)突變在蛋白磷酸化研究中的作用
定點(diǎn)突變可以隨心所欲地改變已知DNA序列中的堿基。在基礎(chǔ)研究中��,科研工作者通常需要通過改變DNA序列獲得突變基因����,以研究基因結(jié)構(gòu)與功能之間的關(guān)系;或者通過改變氨基酸序列獲得突變蛋白��,以研究蛋白質(zhì)結(jié)構(gòu)和功能的關(guān)系�����,從微觀水平闡明生理狀態(tài)下基因的調(diào)控機(jī)理、疾病的病因和發(fā)病機(jī)制����。在磷酸化蛋白的研究中,構(gòu)建模擬磷酸化和非磷酸化的突變實(shí)驗(yàn)是研究磷酸化功能效應(yīng)的一種常用方法���。
1. 磷酸化位點(diǎn)的查找
磷酸化定點(diǎn)突變實(shí)驗(yàn)的第一步首先要查找磷酸化位點(diǎn)�。我們以常用的蛋白數(shù)據(jù)庫UniProt為例說明�����,具體步驟如下:
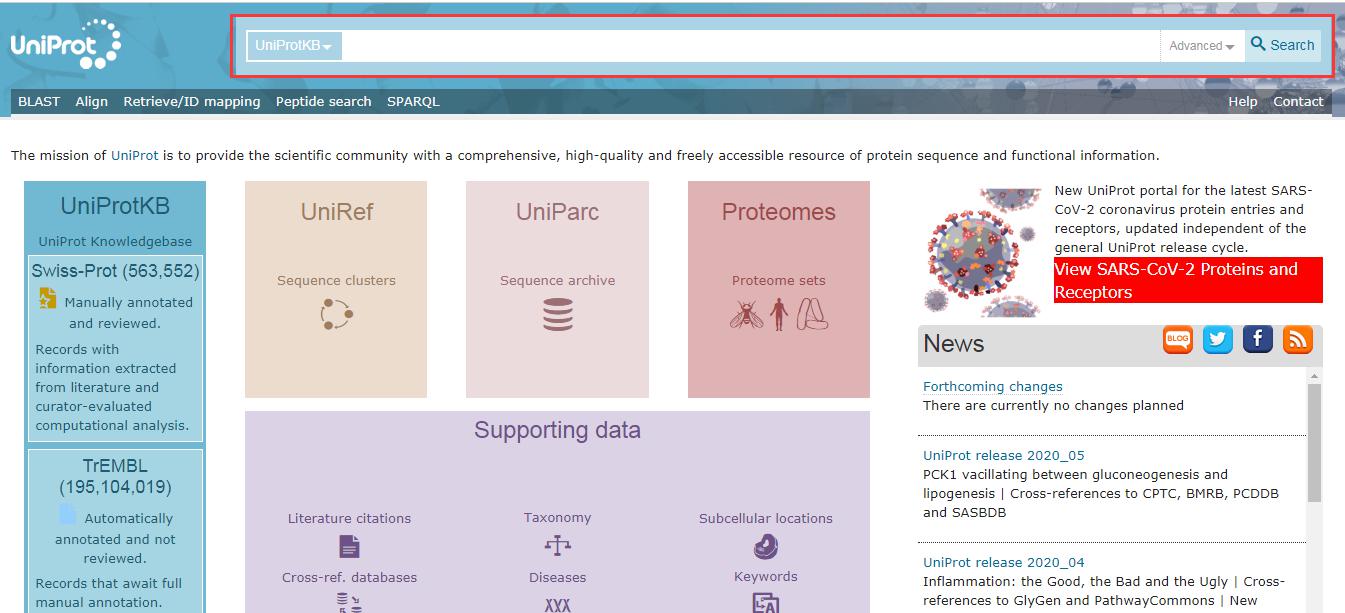
(1)通過https://www.uniprot.org/鏈接進(jìn)入U(xiǎn)niProt官網(wǎng)��,進(jìn)入如下主界面:
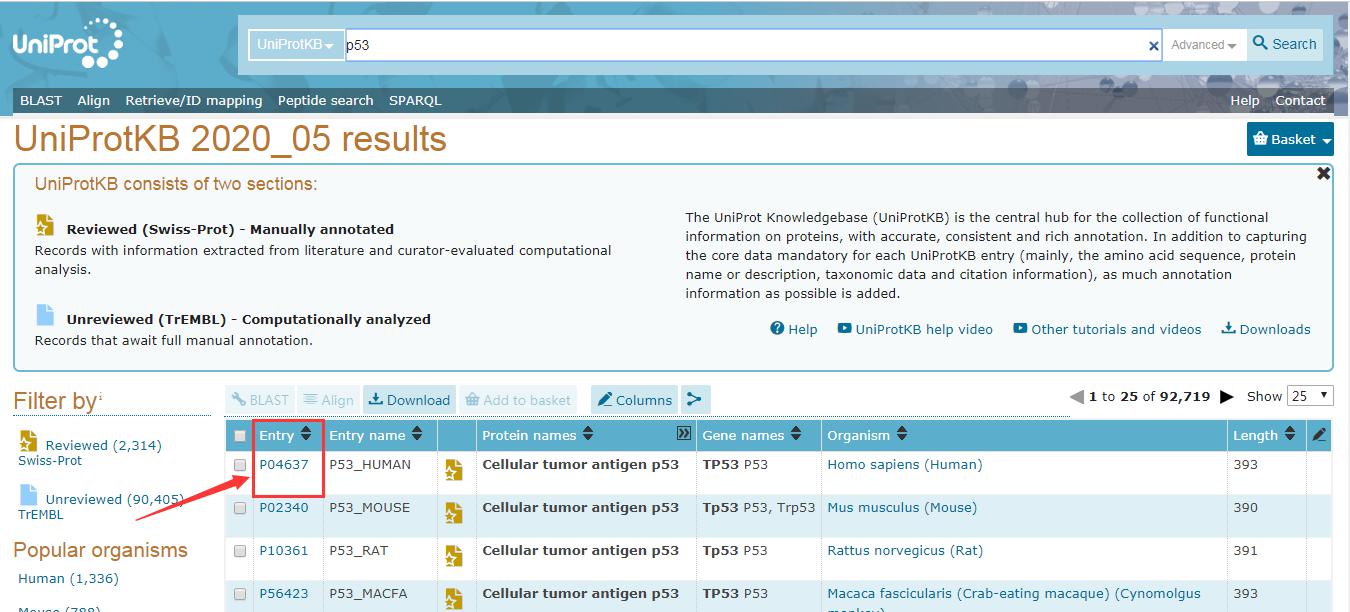
(2)以人源p53蛋白為例����,在Search欄(見上圖紅色標(biāo)記位置)中輸入p53���,進(jìn)入如下界面:
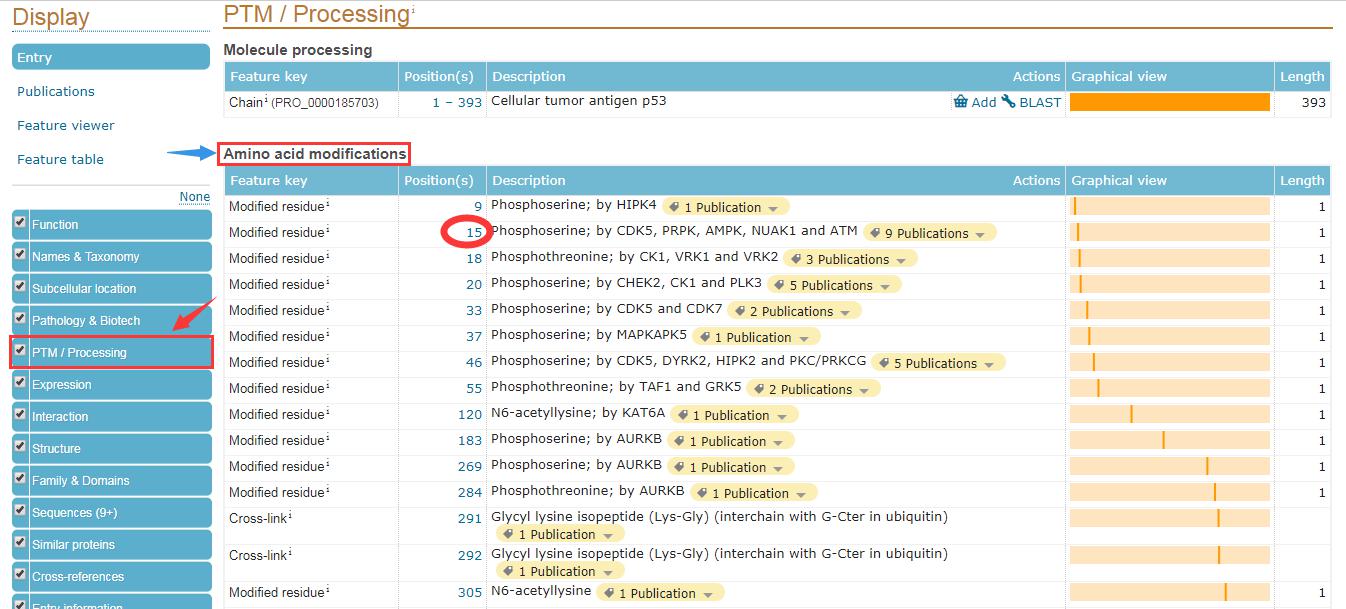
(3)點(diǎn)擊人源p53蛋白在數(shù)據(jù)庫中的編號“Q04637”(上圖紅色箭頭所示),查看專家注釋�。這里重點(diǎn)介紹“PTM/Processing”����。點(diǎn)擊下圖左邊紅色箭頭指向的“PTM/Processing”欄查看分子加工��、氨基酸修飾��、翻譯后修飾、蛋白組學(xué)數(shù)據(jù)庫��、翻譯后修飾數(shù)據(jù)庫和參考文獻(xiàn)。
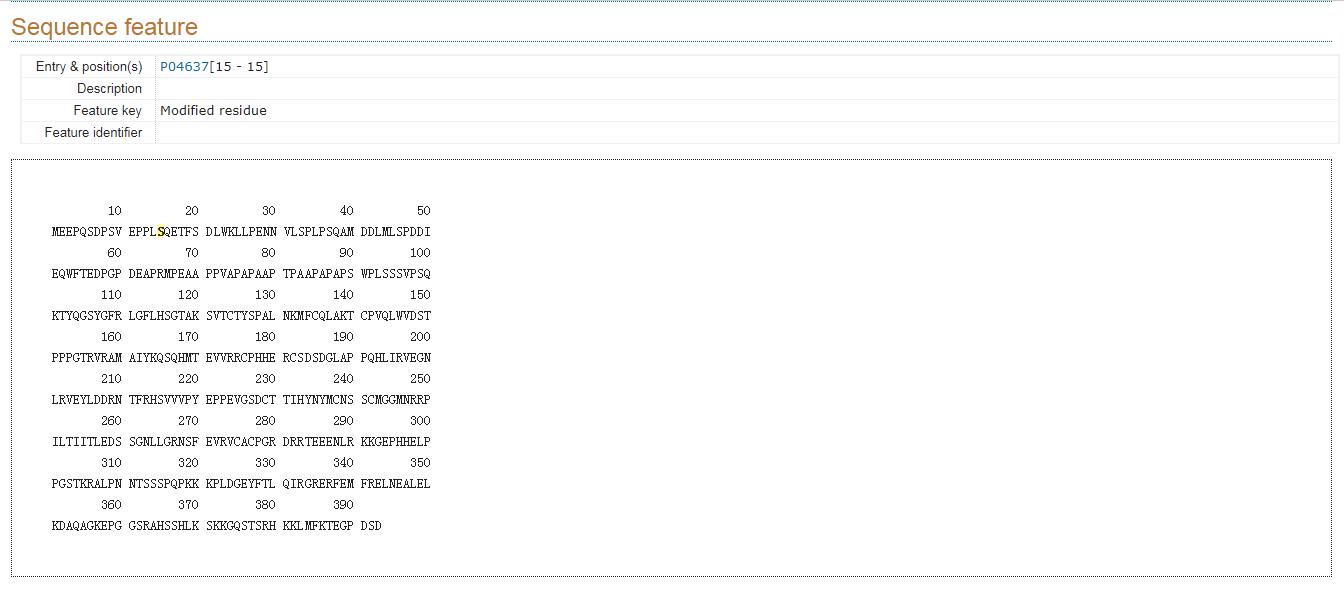
(4)假如我們對15位的磷酸化位點(diǎn)修飾��,點(diǎn)擊紅色圈中的15即可查看對應(yīng)的氨基酸序列(見下圖�����,黃色標(biāo)記的“S”)�。
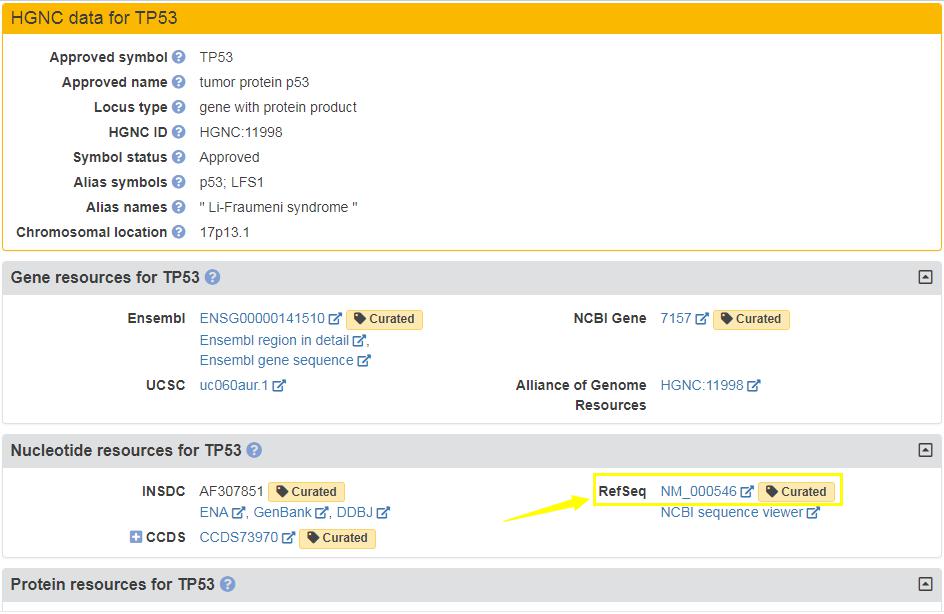
(5)接下來,我們返回上一頁面��,點(diǎn)擊數(shù)據(jù)庫中的“Names & Taxonomy”選項(xiàng)查找該基因的mRNA序列���,點(diǎn)擊藍(lán)色標(biāo)記的基因名即可查閱該基因的詳細(xì)信息�����。
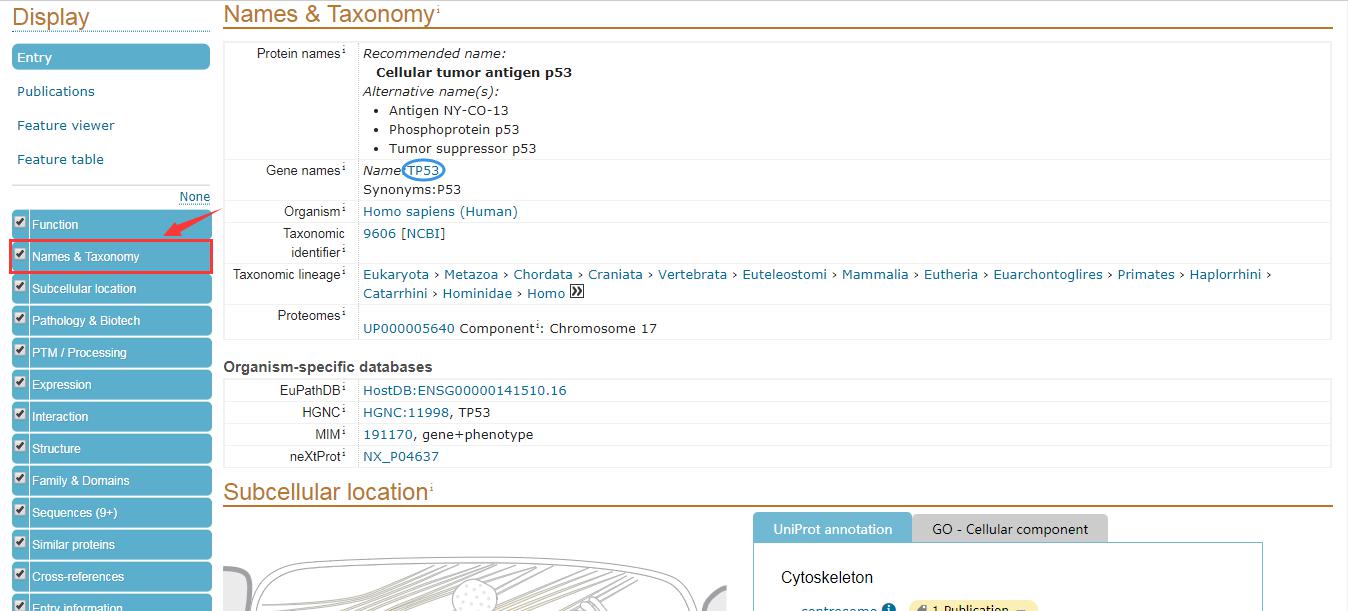
(6)p53的mRNA序列查找可點(diǎn)擊黃色箭頭處獲?���。?/span>
2. 表征磷酸化修飾的定點(diǎn)突變
1)表征磷酸化修飾的突變氨基酸
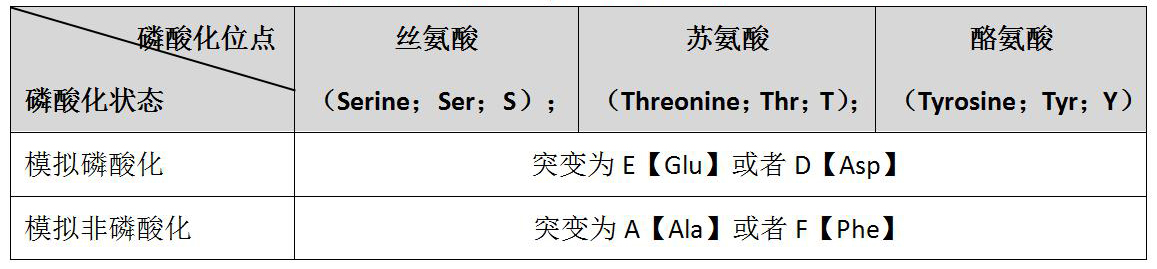
通過第2部分磷酸化類型的介紹�,我們知道Ser�����、Thr和Tyr殘基上的磷酸化較常見�����,特別是Ser。根據(jù)文獻(xiàn)報(bào)道�����,表征這3種磷酸化修飾的定點(diǎn)突變見表3:
表3:表征Ser��、Thr和Tyr磷酸化修飾的突變氨基酸
2)表征磷酸化修飾的原理
蛋白質(zhì)的磷酸化導(dǎo)致磷酸基團(tuán)受體氨基酸殘基上增加了凈負(fù)電荷(pSer�����,pThr和pTyr帶2個負(fù)電荷【見上述圖2】)�����。而取代的酸性氨基酸(Glu和Asp)的負(fù)電荷側(cè)鏈在一定程度上模擬了蛋白質(zhì)中磷酸基團(tuán)的添加��,且長度相似。為了使得實(shí)驗(yàn)結(jié)果準(zhǔn)確���,除了構(gòu)建模擬磷酸化的突變體外,模擬非磷酸化的點(diǎn)突變構(gòu)建也是必需的�,即磷酸基團(tuán)受體氨基酸殘基被一個不帶電的和不能磷酸化的氨基酸殘基所取代����。目前���,Ala和Phe已成功模擬非磷酸化。
3)如何選擇表征磷酸化修飾的突變氨基酸����?
表征磷酸化修飾的突變氨基酸選擇主要從氨基酸的長度����、大小���、電荷和結(jié)構(gòu)方面選擇��。例如�����,與磷酸化的氨基酸殘基相比���,Glu或Asp除了帶1個負(fù)電荷外,還可能占據(jù)更小或不同的空間���。因此�����,在許多情況下�,Glu可能比更小的Ala能更好地模擬pSer���。但是,注意不是所有情況�,這2種氨基酸均已成功模擬pSer。再比如�����,對于非磷酸化的模擬,Ala經(jīng)常被作為取代的氨基酸殘基��。但是�����,對于非磷酸化的Tyr,Phe可能是一個更好的的選擇���。
六.應(yīng)用實(shí)例
實(shí)例一 蛋白磷酸化與肝自噬
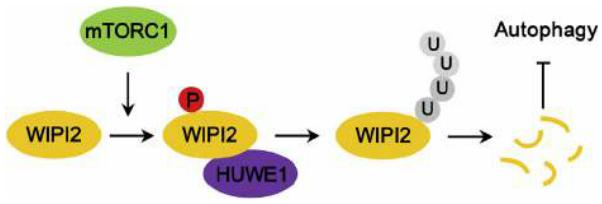
2018年10月���,浙江大學(xué)醫(yī)學(xué)院劉教授課題組在Molecular Cell(IF=15.584)雜志發(fā)表了題為“mTORC1-Regulated and HUWE1-Mediated WIPI2 Degradation Controls Autophagy Flux”研究論文���,該論文從采用質(zhì)譜確定WIPI2新的互作蛋白出發(fā)�����,經(jīng)體內(nèi)外實(shí)驗(yàn)發(fā)現(xiàn)mTORC1 & WIPI2 &HUWE1三者之間的調(diào)控關(guān)系�����、功能效應(yīng)��、生物效應(yīng)和生理功能:WIPI2是mTORC1新的磷酸化底物����。mTORC1通過磷酸化WIPI2����,促進(jìn)WIPI2與其E3泛素連接酶HUWE1的相互作用��,導(dǎo)致WIPI2的泛素化和經(jīng)蛋白酶體的降解,最終抑制自噬���,調(diào)控模型示意圖見圖3���。
圖3:mTORC1 & WIPI2 &HUWE1在細(xì)胞自噬中的調(diào)控示意圖
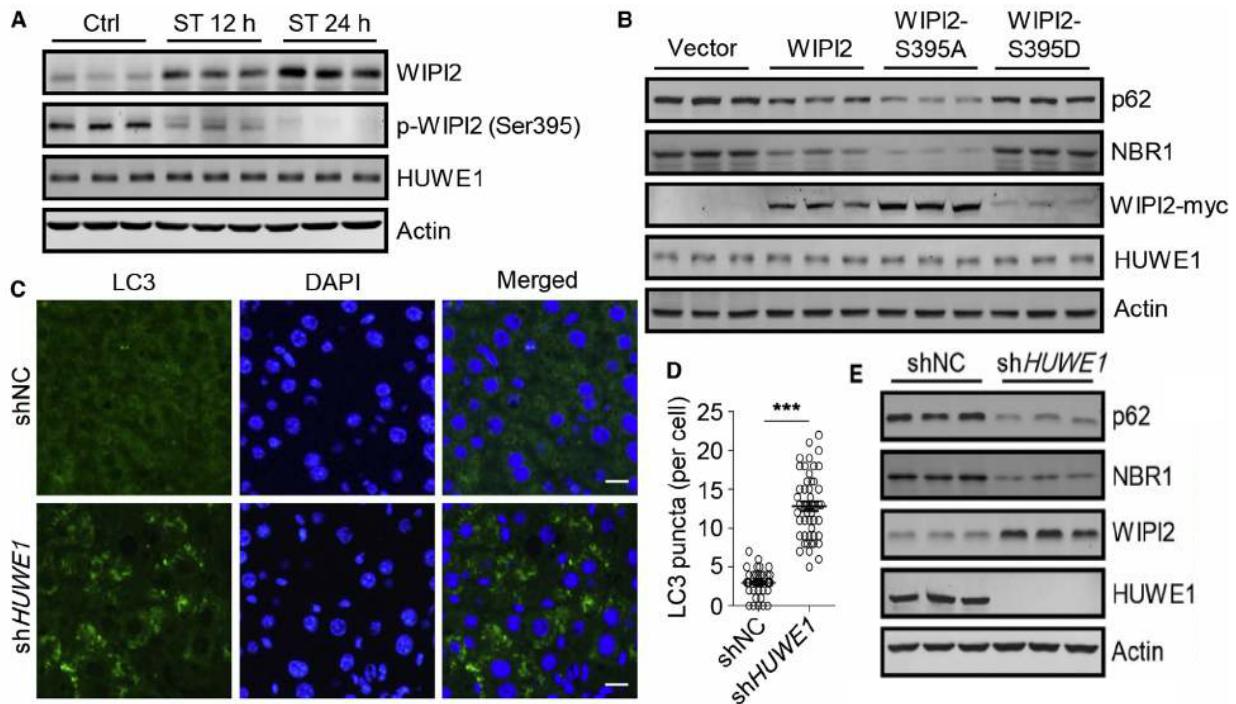
在這里��,我們重點(diǎn)展示作者體內(nèi)生理功能的科研成果�����,這部分研究涉及到模擬磷酸化和非磷酸化突變體的構(gòu)建��,而且非常榮幸的是,本部分研究所用AAV產(chǎn)品由維真生物助力����。首先�����,作者饑餓處理小鼠12h&24h���,通過Western Blot發(fā)現(xiàn)肝臟中的WIPI2蛋白量增加,而磷酸化的WIPI2卻減少�����。為了獲得WIPI2磷酸化調(diào)控小鼠肝自噬的直接證據(jù)����,作者使用rAAV-WIPI2, rAAV-WIPI2-S395A, or rAAV-WIPI2-S395D腹腔注射小鼠�����,4周后發(fā)現(xiàn)WIPI2-S395A蛋白量增加���,而WIPI2-S395D卻減少;而且��,與WT-WIPI2相比���,WIPI2-S395A而不是WIPI2-S395D明顯降低了P62和NBR1的蛋白量。此外,腹腔注射rAAV-shHUWE1的小鼠LC3 puncta、WIPI2的蛋白量和P62&NRB1的降解均表現(xiàn)出了增加(圖4)�����。
圖4:mTORC1介導(dǎo)的WIPI2磷酸化在小鼠肝臟中調(diào)控細(xì)胞自噬
實(shí)驗(yàn)參數(shù)

實(shí)例二 蛋白磷酸化與細(xì)胞遷移、增值和分化
幾乎在同一時間�����,香港浸會大學(xué)的張老師課題組在Cell Death Discov(IF=4.114)雜志發(fā)表了題為“Oleanolic acid enhances neural stem cell migration, proliferation, and differentiation in vitro by inhibiting GSK3βactivity”研究論文,揭示了齊墩果酸(OA)通過抑制GSK3β活性促進(jìn)神經(jīng)干細(xì)胞的遷移����、增殖和分化,此項(xiàng)工作成果對于治療神經(jīng)退行性疾病具有重要的意義�����。
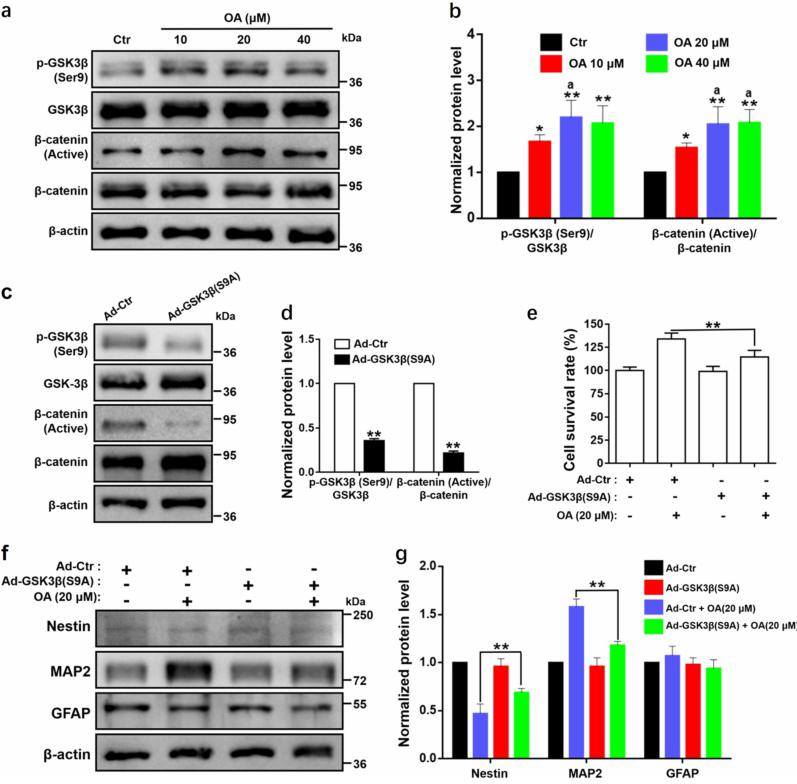
首先,作者通過神經(jīng)球形成實(shí)驗(yàn)證明OA增加NSCs的遷移�����;通過CCK-8實(shí)驗(yàn)和神經(jīng)球形成實(shí)驗(yàn)證實(shí)了OA促進(jìn)NSCs的增殖����;通過western blot和免疫熒光實(shí)驗(yàn)揭示了OA促進(jìn)NSCs分化為神經(jīng)元��。接著��,作者通過分子對接表明GSK3β是OA作用的直接靶基因。最后��,作者通過western blot和構(gòu)建非磷酸化突變體(維真生物助力腺病毒)揭示了本論文主題��,實(shí)驗(yàn)結(jié)果見圖5。
圖5:齊墩果酸(OA)通過抑制GSK3β活性促進(jìn)神經(jīng)干細(xì)胞的增殖和分化
[注:Nestin (NSCs marker);MAP2 (microtubule-associated protein-2, neuron marker)���;GFAP(astrocytes marker)]
實(shí)驗(yàn)參數(shù)
維真生物助力蛋白質(zhì)磷酸化研究
維真生物已建成了18000余種人源基因的現(xiàn)貨克隆庫與12000余種人源基因的腺病毒庫�����,并有蛋白激酶與磷酸酶的克隆子庫���,可為您提供蛋白質(zhì)磷酸化相關(guān)基因的克隆與腺病毒����;我們還建成了靶向13000余種小鼠基因的gRNA pool 克隆庫,同樣地�����,我們也有蛋白磷酸化相關(guān)基因的gRNA pool克隆子庫���,您可直接包裝AAV��,搭配spCas9的轉(zhuǎn)基因小鼠���,完成基因在體內(nèi)的精準(zhǔn)調(diào)控���,所以如果您有基因喪失方向的實(shí)驗(yàn)需求,這款產(chǎn)品將是您的理想選擇���!此外�����,我們還有靶向700余種人源激酶的gRNA慢病毒文庫�,配合CAS9慢病毒或CAS9穩(wěn)定細(xì)胞系���,可實(shí)現(xiàn)快速高通量地篩選。不僅如此��,我們還可以根據(jù)您的實(shí)驗(yàn)需求進(jìn)行磷酸化相關(guān)基因的定點(diǎn)突變���,并為您提供下游的病毒包裝和基因檢測服務(wù)等。
部分產(chǎn)品與服務(wù)如下:
1�、人源蛋白激酶與磷酸酶的現(xiàn)貨克隆子庫
2�、鼠源蛋白激酶與磷酸酶的gRNA pool現(xiàn)貨克隆子庫
3�����、人源蛋白激酶的gRNA慢病毒文庫
4�、人源蛋白激酶與磷酸酶的現(xiàn)貨腺病毒
5、蛋白磷酸化相關(guān)基因定點(diǎn)突變�����、干擾和敲除
6�、蛋白磷酸化相關(guān)基因慢病毒���、腺病毒、AAV包裝
7��、基因的表達(dá)分析服務(wù)...
了解更多產(chǎn)品和服務(wù)��,請咨詢當(dāng)?shù)劁N售經(jīng)理或掃碼聯(lián)系您身邊的小V吧���!