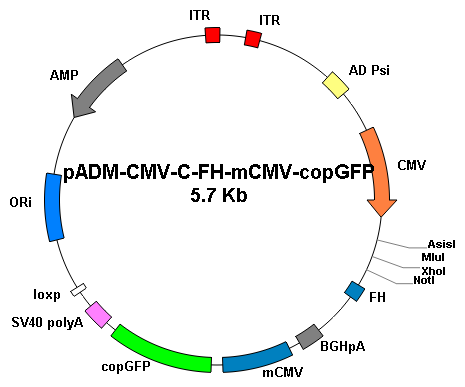
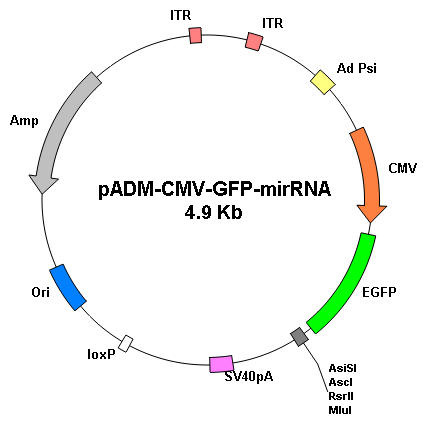
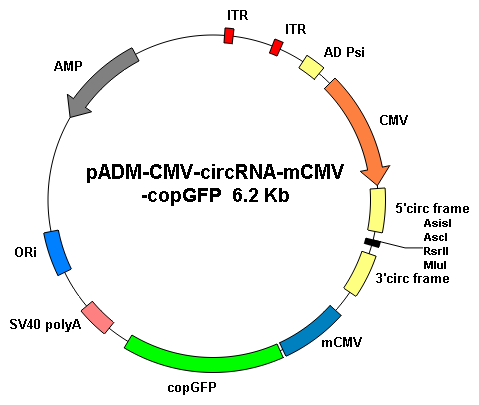
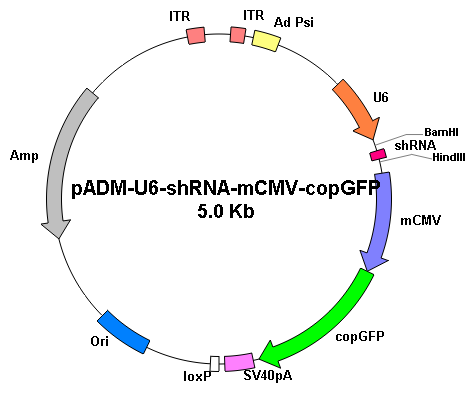
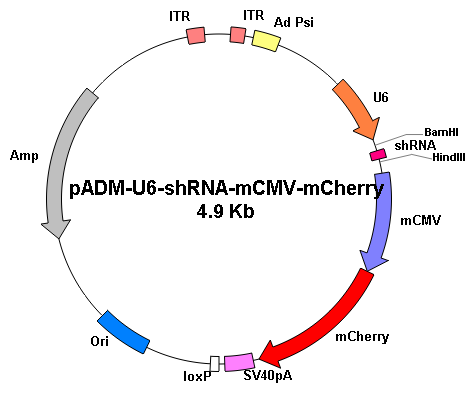
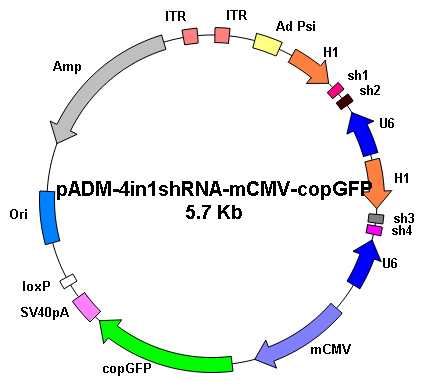
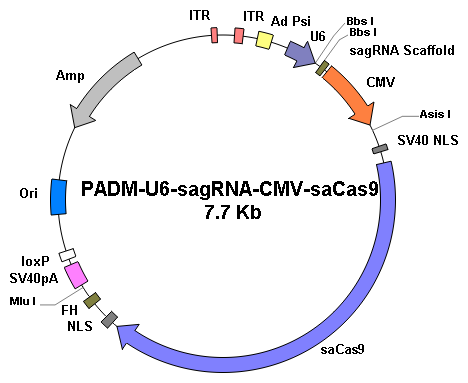
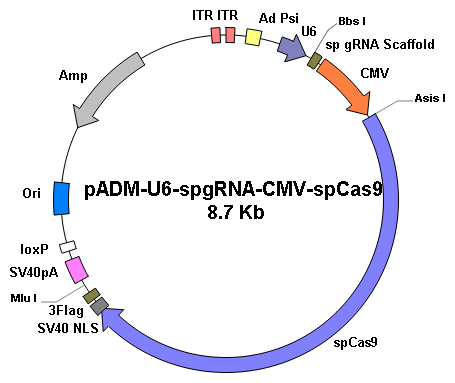
重組腺病毒的制備和使用
1. 重組腺病毒的制備
1.1 細胞轉(zhuǎn)染(以轉(zhuǎn)染 6孔板為例)
① 250μl DMEM和9μl PEI配成Mix1��,靜置5min以上。
② 250μl DMEM和1μg穿梭質(zhì)粒�、2μg包裝質(zhì)粒(即腺病毒骨架質(zhì)粒)���,配成Mix2。
③ 將Mix1和Mix2混合�����,渦旋振蕩混勻����,瞬離后�,靜置30min以上���,以便有充足的時間形成DNA-PEI復(fù)合物���。
④ 靜置期間鋪6孔板HEK293細胞�����,細胞數(shù)約0.3-0.5×106個/孔(也可提前鋪板)�����。
⑤ 將靜置后的混合液逐滴加入至6孔板細胞中。十字混勻后置于CO2培養(yǎng)箱中培養(yǎng)��。
1.2 擴增���、收毒步驟
① 轉(zhuǎn)染后約14天,將六孔板中有CPE的細胞連同培養(yǎng)基吹下加入至10cm dish�,混勻后置于 CO2培養(yǎng)箱中培養(yǎng)���。
② 收集有CPE的10cm dish細胞,用電動移液器轉(zhuǎn)移至 15mL離心管中�����,并做好相應(yīng)的標(biāo)記;
③ 3500rpm,離心7min����;離心完成后,取出離心管����,保留細胞沉淀�,并將上清保存至其他離心管中備用�����。
④ 在細胞沉淀中加入腺病毒凍存液�,用移液槍不斷地吹打沉淀����,保證完全回溶�,吸到1.5mL EP管中。
⑤ -80℃及 37℃反復(fù)凍融四次����。
⑥ 凍融完成后����,12000g離心2min。
⑦ 將上清用1mL槍移到二維碼管中����,存放于-80℃的冰箱中�。
1.3 大量擴增及收毒步驟
① 將收集起來的病毒上清平均滴加到10個10cm dish中���,混勻后置于CO2培養(yǎng)箱中培養(yǎng),2-3天后收毒����;
② 收集有CPE的10個10cm dish細胞,用電動移液器轉(zhuǎn)移至50ml離心管中���,并做好相應(yīng)的標(biāo)記��;
③ 3500rpm,離心7min��,分別收集上清和細胞沉淀����;
④ 病毒上清加入PEG8000和NaCl,混勻后4℃直立放置過夜����;細胞沉淀置于-80℃保存?zhèn)溆谩?
1.4 純化前的處理
① 病毒上清處理
a. 第二天將4℃過夜的上清離心���,3500g,4℃����,離心 30min��;
b. 離心后棄掉上清��,收集病毒沉淀;
c. 用2mL凍存液將病毒沉淀重懸���,收集到15ml管中備用��。
② 細胞沉淀處理
a. 細胞沉淀用6mL腺病毒凍存液重懸�,混勻�����,反復(fù)凍融四次;
b. 凍融完畢后����,3500g�����,4℃��,離心30min���,分別收集上清和沉淀(細胞碎片)��;
c.上清與重懸后的病毒沉淀混合����;細胞碎片用2mL凍存液進行重懸���;
③ 超聲波破碎細胞
a. 重懸后的細胞碎片超聲波破碎3-4次�����,至液體不粘稠;
b. 超聲完畢后����,將液體分裝到2個EP管中��,12000g,4℃離心10min;
c. 離心完成后�����,與病毒上清和細胞沉淀處理后的樣品混合�。
1.5 純化與濃縮
① 純化——碘克沙醇密度梯度離心����。
a. 配制不同濃度的碘克沙醇;
b. 取一個超離管���,用電動移液器逐層、緩慢加入不同濃度的碘克沙醇��;
c. 將處理好的病毒液加入到最上層�;
d. 超速離心,48000rpm��,2h30min。離心前應(yīng)將對應(yīng)的超離管配平�,誤差控制在0.1g以內(nèi)��。
② 濃縮
a. 離心完畢后����,將超離管底用針頭刺破�,收集腺病毒所在層至15mL管中����;
b. 將收集的病毒液用凍存緩沖液稀釋至體積15mL��,然后用0.2μm的濾膜過濾�;
c. 將過濾后的液體置于一個15mL的超濾管中����,3500g離心50min進行濃縮,一般離心2-3次后達到預(yù)定體積;
d. 將超濾管中剩下的液體反復(fù)吹打后吸至病毒儲存管中���,標(biāo)明名稱和日期。
e. 將收集起來的病毒渦旋震蕩混勻后離心�,吸10μL病毒液進行滴度檢測�。
1.6 病毒滴度檢測
實時定量PCR法是一種簡單的����、高通量的測定病毒粗提裂解液和純化病毒樣本中腺病毒顆粒數(shù)量的方法�。每個模板的Ct值與該模板起始拷貝數(shù)的對數(shù)存在線性關(guān)系�����,利用已知起始拷貝數(shù)的標(biāo)準(zhǔn)品可作出標(biāo)準(zhǔn)曲線���,最后通過標(biāo)準(zhǔn)曲線對未知模板進行定量分析�����。
① 去除游離DNA分子
先將病毒稀釋10倍,以保證樣品中游離的DNA充分降解:取5μl病毒至45μl PBS緩沖液中����,充分混勻���。按以下體系配制Mixture:
|
組成成分
|
體積
|
|
超純水(DNase & RNase Free)
|
4 μl
|
|
DNAaseI
|
1 μl
|
|
10×DNAaseI Buffer
|
1μl
|
|
病毒稀釋液
|
4μl
|
|
Total
|
10μl
|
37℃ 孵育30 min,95℃加熱5min使DNA酶失活���。
② 去除病毒蛋白外殼
向上述體系中再加入 1μl蛋白酶K(5μg/μl)��。37℃ 孵育30 min����;再加30ul超純水稀釋至40ul(至此病毒原液稀釋100倍)���,95℃加熱5 min使蛋白酶K失活,然后12000rpm����,離心2min,取上清進行qPCR檢測��。
③ qPCR
將步驟2得到的上清���,取5μl進行10倍梯度稀釋��,即病毒原液稀釋了1000倍。分別取2μl待測樣品及標(biāo)準(zhǔn)品作為模板進行qPCR檢測。
qPCR反應(yīng)體系如下:
|
組成成分
|
體積
|
|
2 × SYBR Green mix
|
10μl
|
|
Primers (Forward & Reverse mixture)
|
0.8 μl
|
|
超純水(DNase & RNase Free)
|
7.2μl
|
|
DNA
|
2μl
|
|
Total
|
20μl
|
qPCR反應(yīng)程序:
|
循環(huán)參數(shù)
|
|
預(yù)變性95℃
|
3min
|
|
95℃
|
5S
|
|
60℃
|
15S
|
|
72℃
|
15S+Plate Read
|
|
39個循環(huán)
|
④ 數(shù)據(jù)分析
病毒顆粒數(shù)的計算:病毒顆粒數(shù)(VP/mL) =與標(biāo)準(zhǔn)品相對值×1000
2. 重組腺病毒的使用
2.1 腺病毒體外感染細胞
① 腺病毒感染目的細胞預(yù)實驗
不同細胞系細胞表面的腺病毒受體數(shù)量不同,這就決定了不同細胞系所使用的MOI會有所不同�����。通常,易感染細胞系所使用的MOI范圍為10-100�����。 但是,對于某些難感染的細胞系�,MOI可能需要高達1000���。對于大多數(shù)細胞系來說����,最佳MOI的范圍很窄�����。我們建議您查閱文獻或者在正式實驗前,在目的細胞中用報告基因的腺病毒進行預(yù)實驗摸最佳MOI。
為了節(jié)省病毒����,推薦使用96孔板進行預(yù)實驗����。操作步驟如下:
a. 第一天細胞的準(zhǔn)備
將目的細胞接種于96孔板中����,細胞融合率為50%較佳。為保證細胞生長良好��,請保證細
胞貼壁過夜。
b. 第二天病毒的稀釋
取 10μL腺病毒原液加入90μL培養(yǎng)液中做1:10稀釋(10-1)����,以此為起點做梯度稀釋直至稀釋10-7?����?筛鶕?jù)實際情況降低或提高稀釋倍數(shù)。
c. 第二天感染目的細胞
取出提前準(zhǔn)備好的96孔板��,用準(zhǔn)備好的病毒稀釋液替代舊培養(yǎng)液����,注意保留未加入病毒的
細胞孔作為對照組。
d. 第二至四天觀察熒光或檢測
腺病毒對細胞的感染較快,請在感染細胞后12��、24、36���、48小時分別觀察細胞中熒光表達
情況(如果您選擇的產(chǎn)品不帶有熒光標(biāo)簽�,請在 48��、72、96���、120小時分別收獲細胞并通
過 Western-Blot或其他檢測手段來檢測基因表達)。
|
注意:
|
感染前細胞的狀態(tài)好壞對最終的感染效果高低影響很大�����,請務(wù)必保證加入病毒前, 細胞處于良好的生長狀態(tài)����。
|
|
② 腺病毒感染目的細胞實驗
進行腺病毒感染實驗時可使用完全培養(yǎng)液(培養(yǎng)目的細胞用)稀釋��。培養(yǎng)液中的血清、雙抗或其他營養(yǎng)因子不會影響腺病毒的感染效率�。
以 24孔培養(yǎng)板為例,進行HEK293細胞的感染實驗操作步驟如下:
|
注意:
|
實驗前請按照不同的 MOI設(shè)置不同的感染孔,并根據(jù)MOI和細胞數(shù)量計算所需要的病毒量�����。
|
|
最適病毒用量的計算公式:
病毒用量pfu=最佳MOI×細胞數(shù)目/病毒滴度
例如,如果您目的細胞的最佳MOI=10,您需要感染106的細胞,那么您共計需要107pfu的病毒.如果病毒滴度為1×1010 pfu/mL,那么您實驗需要的病毒量就是1ul.
a. 第一天細胞的準(zhǔn)備
在24孔培養(yǎng)板接種若干孔���,每個孔內(nèi)接種3-5×104個 HEK 293細胞,鋪板時細胞的融合率為50%左右��,每孔培養(yǎng)液體積為300μL(進行病毒感染時細胞的匯合度約為70% )。
b. 第二天病毒的準(zhǔn)備
根據(jù)實驗的實際情況和MOI值���,用培養(yǎng)液準(zhǔn)確稀釋腺病毒原液����。
注意事項:可使用 PBS緩沖液或無血清培養(yǎng)液稀釋病毒原液�����。
c. 第二天感染目的細胞
在目的細胞和對照細胞中分別加入計算好的病毒液,混勻后放于CO2培養(yǎng)箱(37℃、
5% CO2)孵育過夜。
|
注意:
|
1)感染前細胞的狀態(tài)好壞對感染效率影響很大,請務(wù)必保證加入病毒前��,細胞處于良好 的生長狀態(tài)����。
2)若病毒對目的細胞的感染效率較低,可通過提高MOI值提高病毒的感染效率�����,也可 在培養(yǎng)液中加入維真生物的助感染試劑ADV-HR來提高病毒的感染效率。
|
|
d. 第三天更換培養(yǎng)液
病毒感染細胞12小時后���,更換培養(yǎng)液��。
|
注意:
|
換液具體時間需視細胞狀態(tài)而定��。如果腺病毒對細胞有明顯毒性作用��,影響細胞生 長狀態(tài),最短可于加病毒4小時后更換新鮮培養(yǎng)液�����。
|
|
e. 第三天感染效率檢測
感染 24小時后��,可利用倒置熒光顯微鏡觀察病毒感染目的細胞的效率。如選擇的腺病毒載
體不帶有熒光標(biāo)記�����,可以通過Q-PCR(定量PCR)檢測目的基因的表達來評估感染效率����。
|
耗材名稱
|
貨號
|
品牌
|
|
細胞培養(yǎng)板 10cm
|
704001
|
NEST
|
|
細胞培養(yǎng)板 15cm
|
715001
|
NEST
|
|
10ml血清移液管
|
4488
|
Corning
|
|
50ml血清移液管
|
4490
|
Corning
|
|
100-1250無菌加長帶刻度濾芯槍頭
|
TF112-1000-Q
|
QSP
|
|
細胞凍存管
|
377267
|
Corning
|
|
DMEM高糖培養(yǎng)基
|
C11965500BT
|
GIBICO
|
|
HEPES溶液 1M
|
SH30237.01
|
HyClone
|
|
青霉素-鏈霉素溶液(100*)
|
C0222
|
碧云天
|
|
胎牛血清
|
1122050
|
Gibico
|
|
0.25%胰蛋白酶
|
SH30042.01
|
Hyclone
|
|
10xPBS
|
ST476
|
碧云天
|
|
DMSO
|
D8372
|
SOLARBIO
|
|
儀器名稱
|
規(guī)格型號
|
品牌
|
|
生物安全柜
|
BSC-1300IIA2
|
蘇凈集團蘇州安泰空氣技術(shù)有限公司
|
|
倒置顯微鏡
|
CKX31SF
|
OLYMPUS
|
|
二氧化碳培養(yǎng)箱
|
MCO-15AC
|
三洋電機株式會社
|
|
實時熒光定量擴增儀(QPCR儀)
|
CFX96
|
BIO-RAD
|
|
熒光顯微鏡
|
ELWD0.3
|
Nikon
|
|
超低溫保存箱
|
DW-86L386
|
青島海爾特種儀器有限公司
|
|
臺式高速冷凍離心機
|
1580R
|
LAB GENE 基因有限公司
|